Белок NUDT5 контролирует синтез ДНК необычным способом
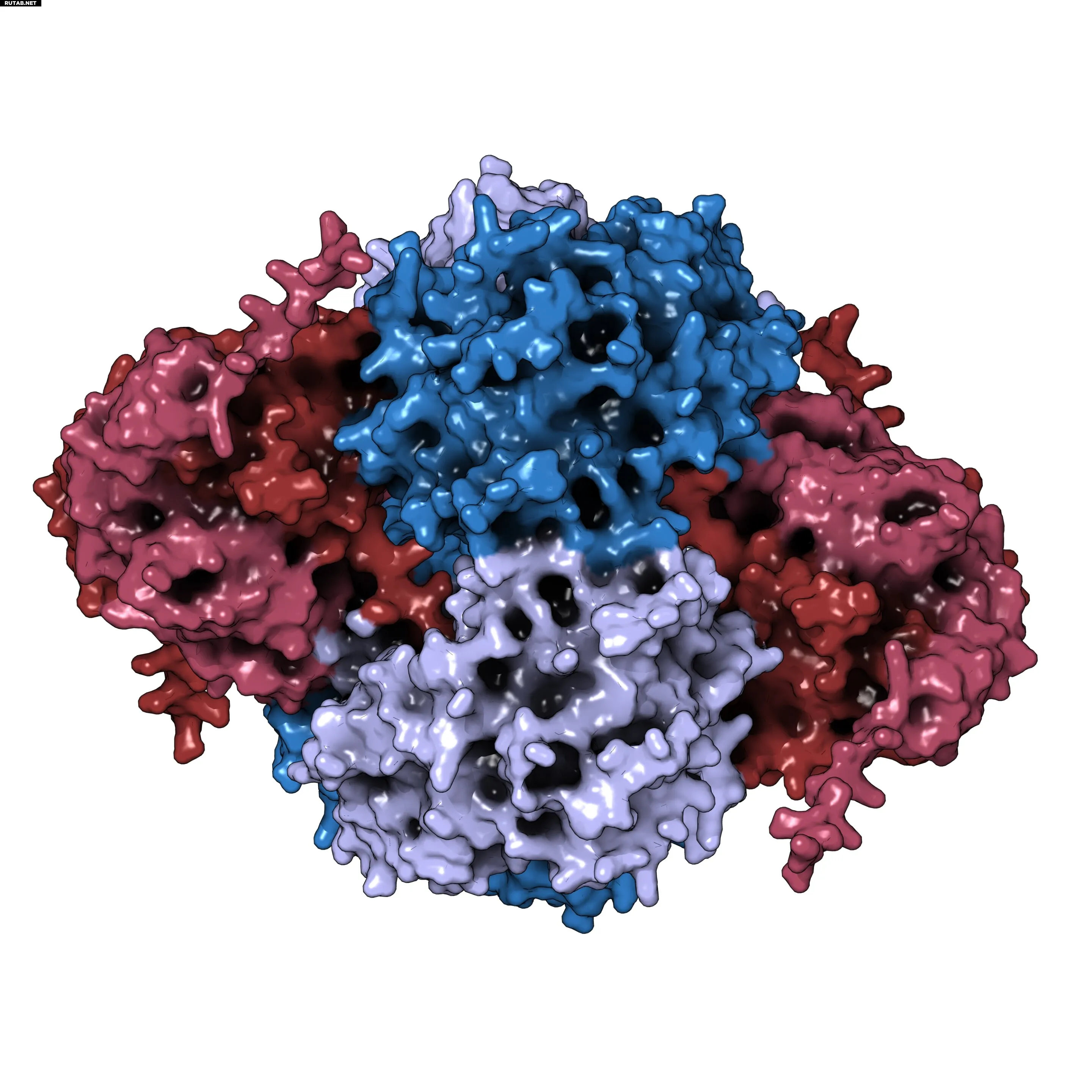
Предсказанная структура взаимодействия димеров NUDT5 (красный) и тетрамера PPAT (синий). Автор: Туан-Ань Нгуен
Ученые из CeMM (Исследовательского центра молекулярной медицины Австрийской академии наук) и Оксфордского университета обнаружили неожиданную роль белка NUDT5 в метаболизме клетки. Исследование, опубликованное в журнале Science, показывает, что NUDT5 помогает «выключать» производство пуринов — химических соединений, являющихся строительными блоками ДНК, — но делает это без использования своей ферментативной активности.
Вместо катализа химических реакций белок действует как молекулярный каркас, который физически блокирует ключевой этап биосинтеза, когда уровень пуринов в клетке уже высок.
Новая функция известного белка
Пурины необходимы клеткам для построения ДНК и РНК, а также для хранения энергии. Их можно рециркулировать из существующего материала или производить «с нуля» через энергоемкий процесс, который должен строго контролироваться.
Исследователи обнаружили, что NUDT5 взаимодействует с ферментом PPAT, катализирующим первый этап синтеза пуринов. При повышении уровня пуринов NUDT5 связывается с PPAT и, вероятно, переводит его в неактивную форму, давая клетке сигнал прекратить производство.
Удивительно, но эта функция NUDT5 не зависит от его известной ферментативной активности. Даже когда каталитический участок белка был химически заблокирован или инактивирован генетически, белок продолжал регулировать синтез пуринов. Только полное удаление NUDT5 из клетки лишало ее этого контрольного механизма.
Медицинские последствия открытия
Открытие проливает новый свет на то, как клетки ощущают и реагируют на изменения в своей метаболической среде.
«NUDT5 давно классифицировали как фермент, расщепляющий метаболиты, — говорит Стефан Кубичек, главный исследователь CeMM и старший автор работы. — Но наша работа раскрывает совершенно другую роль — он действует как структурный регулятор, который определяет, будет ли клетка продолжать производить пурины или нет».
Этот механизм может объяснить, почему некоторые клетки становятся устойчивыми к определенным противораковым препаратам.
«Многие химиотерапевтические средства, такие как 6-тиогуанин, работают, имитируя молекулы пуринов и блокируя синтез ДНК, — объясняет Туан-Ань Нгуен, соавтор исследования. — Но мы обнаружили, что клетки без функционального взаимодействия NUDT5–PPAT были менее чувствительны к этим методам лечения, что позволяет предположить, что мутации в NUDT5 могут способствовать лекарственной устойчивости опухолей».
Коллеги из лаборатории Килиана Хубера в Оксфорде также разработали химический деградер под названием dNUDT5, который может селективно удалять NUDT5 из клеток. Этот инструмент позволит ученым более детально изучить данный путь и может предложить будущие возможности для защиты здоровых клеток от побочных эффектов химиотерапии.
Дополнительная информация: Jung-Ming G. Lin et al, A non-enzymatic role of Nudix hydrolase 5 in repressing purine de novo synthesis, Science (2025). DOI: 10.1126/science.adv4257






0 комментариев