CRISPR-Cas3: новая система редактирования генома для лечения наследственных заболеваний
Учёные из Токийского университета оценили потенциал системы редактирования генома CRISPR–Cas3 для лечения транстиретинового амилоидоза (ATTR) — прогрессирующего наследственного заболевания, поражающего сердце и нервы. Результаты исследования опубликованы в журнале Nature Biotechnology.
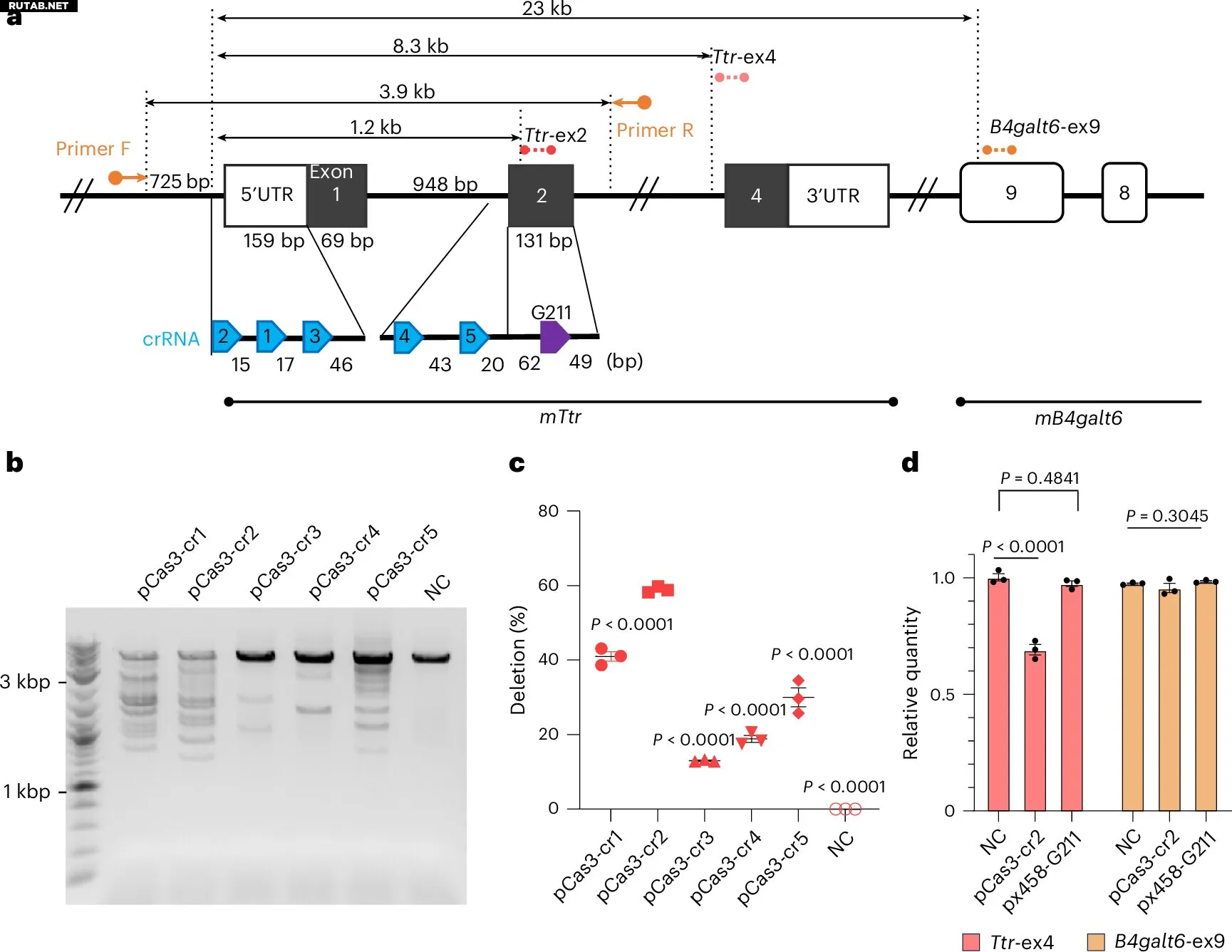
Скрининг crRNA, нацеленной на ген Ttr в клетках мыши Hepa1-6. Автор: Nature Biotechnology (2026). DOI: 10.1038/s41587-025-02949-6
В отличие от широко известной системы CRISPR–Cas9, которая действует как «молекулярные ножницы», делая точные разрезы в ДНК, CRISPR–Cas3 работает иначе. Она использует комплекс белков, который направляет фермент Cas3 для «разрубания» и удаления больших участков ДНК в одном направлении.
Используя модель мыши с ATTR и систему доставки на основе липидных наночастиц (LNP), исследователи под руководством профессора Томодзи Масимо и доктора Саэко Исиды добились многообещающих результатов. В экспериментах на клетках редактирование гена TTR достигло 59%, а однократное введение мышам позволило отредактировать более 48% гена в печени и снизить уровень белка TTR в сыворотке крови на 80%.
«Редактирование генома обладает уникальным потенциалом для коррекции генетических аномалий, связанных с наследственными заболеваниями. Мы хотели выяснить, можно ли разработать систему CRISPR–Cas3 как эффективный терапевтический инструмент», — пояснил профессор Масимо.
Важным преимуществом новой системы стало отсутствие нецелевых мутаций (инделов) в проверенных участках генома, что является серьёзным ограничением для CRISPR–Cas9. Это снижает риск образования непреднамеренных, потенциально вредных белков.
Учёные считают, что после дальнейшей оптимизации и проверки безопасности CRISPR–Cas3 может стать новой и более безопасной платформой для генной терапии, предлагая пациентам с наследственными заболеваниями долговременное, возможно, однократное лечение, устраняющее первопричину болезни.
«В ближайшие годы эта технология может найти клиническое применение не только для ATTR, но и для других в настоящее время неизлечимых наследственных заболеваний», — отметил профессор Масимо.
Исследование финансировалось за счёт грантов Японского агентства медицинских исследований и разработок (AMED) и Японского общества содействия науке (JSPS).

0 комментариев