Новый наноматериал использует окислительный стресс для уничтожения раковых клеток
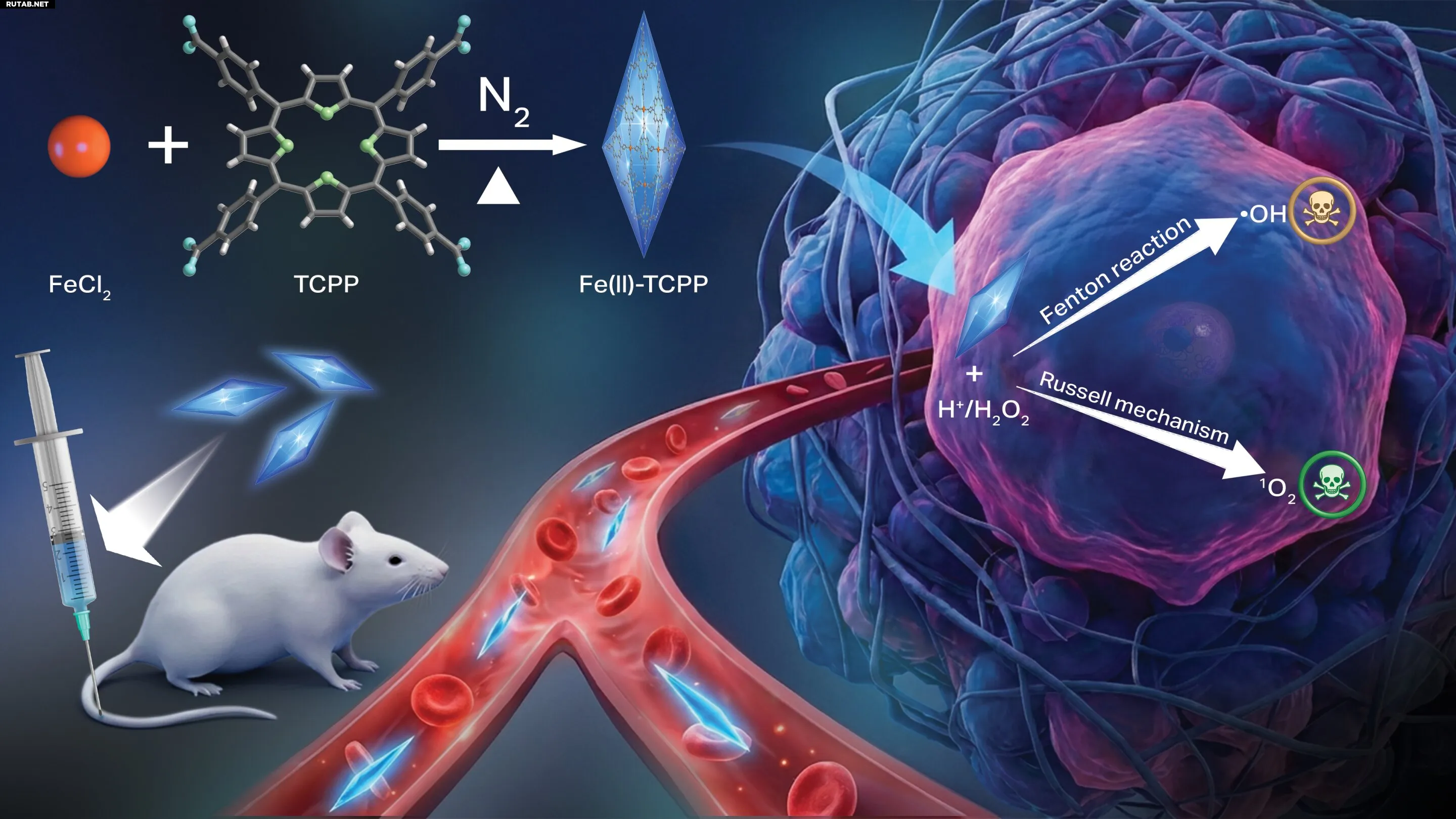
Учёные из Университета штата Орегон разработали новый наноматериал, который запускает пару химических реакций внутри раковых клеток, убивая их посредством окислительного стресса, при этом не затрагивая здоровые ткани. Это металлоорганический каркас на основе железа, который в раковых клетках катализирует производство радикальных гидроксилов и синглетного кислорода. Автор: Париназ Ганбари
Учёные из Университета штата Орегон разработали новый наноматериал, который запускает пару химических реакций внутри раковых клеток, убивая их посредством окислительного стресса, при этом не затрагивая здоровые ткани. Исследование под руководством Олега и Елены Таравула и Чао Вана из Фармацевтического колледжа Университета штата Орегон опубликовано в журнале Advanced Functional Materials.
Эти выводы продвигают область химиодинамической терапии (ХДТ) — нового подхода к лечению, основанного на отличительной биохимической среде, обнаруженной в раковых клетках. По сравнению со здоровыми тканями, злокачественные опухоли более кислые и имеют повышенные концентрации перекиси водорода, объясняют учёные.
Обычная ХДТ работает за счёт использования микроокружения опухоли для запуска химического производства гидроксильных радикалов — молекул, состоящих из кислорода и водорода, с неспаренным электроном. Эти активные формы кислорода способны повреждать клетки через окисление, отбирая электроны у таких молекул, как липиды, белки и ДНК.
Современные разработки в области химиодинамической терапии позволили использовать условия опухоли для катализирования производства другой активной формы кислорода — синглетного кислорода, названного так потому, что у него одно спиновое состояние электрона, в отличие от трёх состояний, обнаруженных в более стабильных молекулах кислорода в воздухе.
«Однако существующие агенты ХДТ ограничены, — сказал Олег Таравула. — Они эффективно генерируют либо радикальные гидроксилы, либо синглетный кислород, но не оба сразу, и им часто не хватает достаточной каталитической активности для поддержания устойчивого производства активных форм кислорода. Как следствие, доклинические исследования часто показывают лишь частичную регрессию опухоли, а не устойчивый терапевтический эффект».
В этой статье учёные представляют новый наноагент ХДТ — металлоорганический каркас (MOF) на основе железа, способный генерировать оба соединения для более эффективного лечения и обладающий превосходной каталитической эффективностью. MOF продемонстрировал мощную токсичность в отношении нескольких линий раковых клеток и незначительный вред для нераковых клеток.
«Когда мы системно вводили наш наноагент мышам с человеческими клетками рака молочной железы, он эффективно накапливался в опухолях, активно генерировал активные формы кислорода и полностью уничтожал рак без побочных эффектов, — добавила Елена Таравула. — Мы наблюдали полную регрессию опухоли и долгосрочное предотвращение рецидива, и всё это без какой-либо системной токсичности».
Прежде чем это лечение можно будет испытать на людях, исследовательская группа планирует оценить его терапевтическую эффективность при различных типах рака, включая агрессивный рак поджелудочной железы, чтобы продемонстрировать его широкую применимость при различных злокачественных новообразованиях.
Источник: Oregon State University












0 комментариев