Ученые раскрыли механизм работы обезболивающих на молекулярном уровне
Исследователи из Детской исследовательской больницы Сент-Джуд объяснили, как разные лекарства, воздействующие на один и тот же клеточный рецептор, вызывают сигналы разной силы. Это открытие может помочь в создании более безопасных и эффективных обезболивающих препаратов.
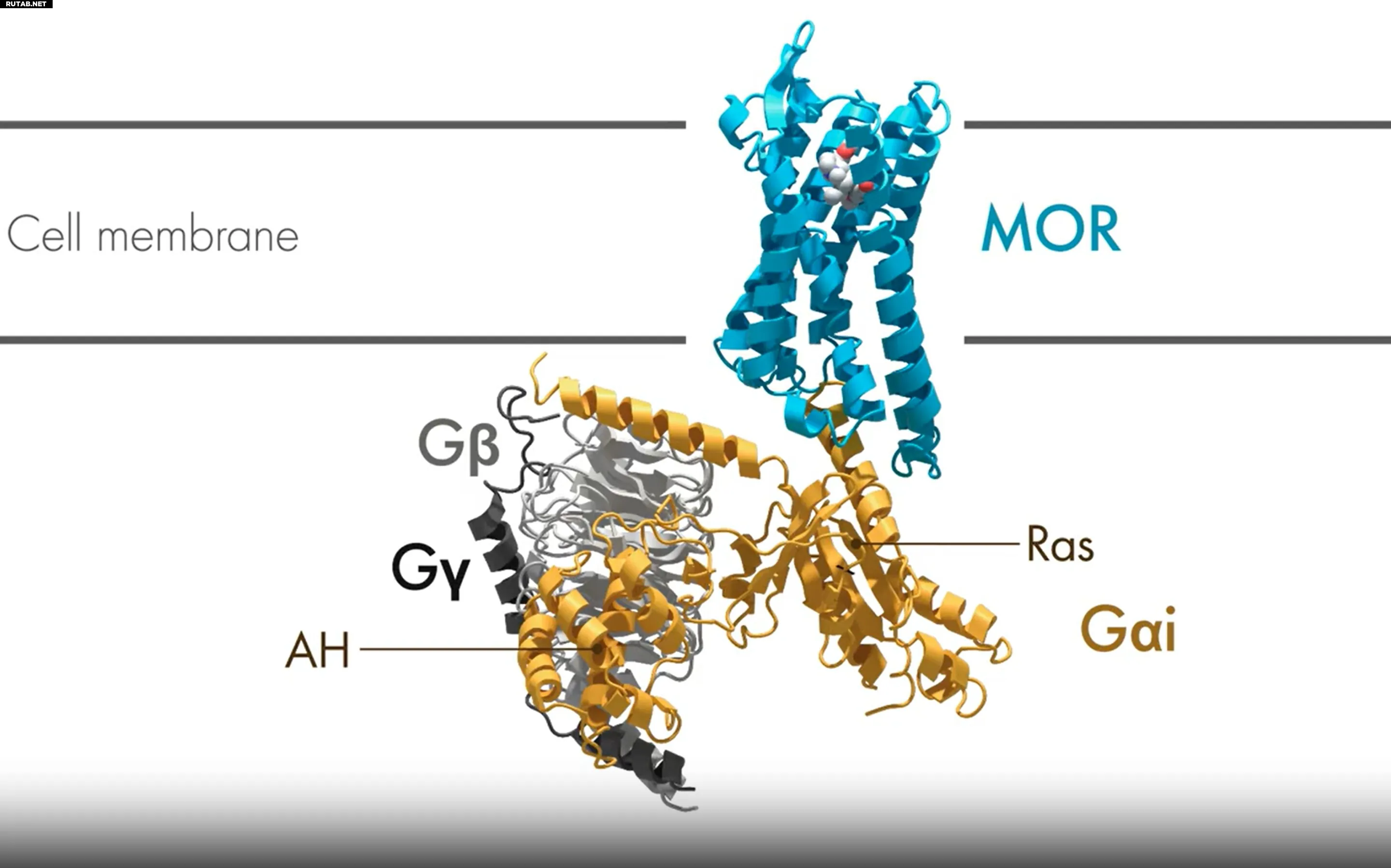
Речь идет о G-белок-сопряженных рецепторах (GPCR), которые передают сигналы внутрь клетки. Мю-опиоидный рецептор, на который действуют такие препараты, как морфин и кодеин, является одним из них. Ученые давно пытались понять, почему разные вещества-агонисты, связываясь с одним рецептором, активируют его с разной интенсивностью.
Используя криоэлектронную микроскопию, команда смогла получить «молекулярные фильмы», показывающие процесс активации рецептора под действием трех разных типов агонистов: частичного, полного и суперагониста.
Оказалось, что ключевую роль играет так называемая «кинетическая ловушка». Активация рецептора — это серия изменений его формы. Полные и суперагонисты быстро «проталкивают» рецептор через все промежуточные состояния, подобно тяжелому шару, катящемуся с горы. Частичные агонисты застревают в этих промежуточных формах, особенно ближе к концу процесса, что замедляет передачу сигнала.
«Мы показали, что разные агонисты действуют как разные люди, толкающие липкий диммер-выключатель. Все переводят его из положения "выключено" в "включено", но более сильные делают это быстрее, а более слабые замедляются или "застревают" на особенно липких участках пути», — пояснил руководитель исследования Георгиос Скиниотис.
Это открытие объясняет, почему частичные агонисты в итоге также активируют рецептор, но делают это медленнее и с меньшей эффективностью. Понимание этих динамических процессов может помочь в разработке лекарств нового поколения, которые будут максимально эффективными при минимальных побочных эффектах.
Исследование опубликовано в журнале Nature.






0 комментариев