Учёные раскрыли механизм адаптации клеток к нехватке кислорода
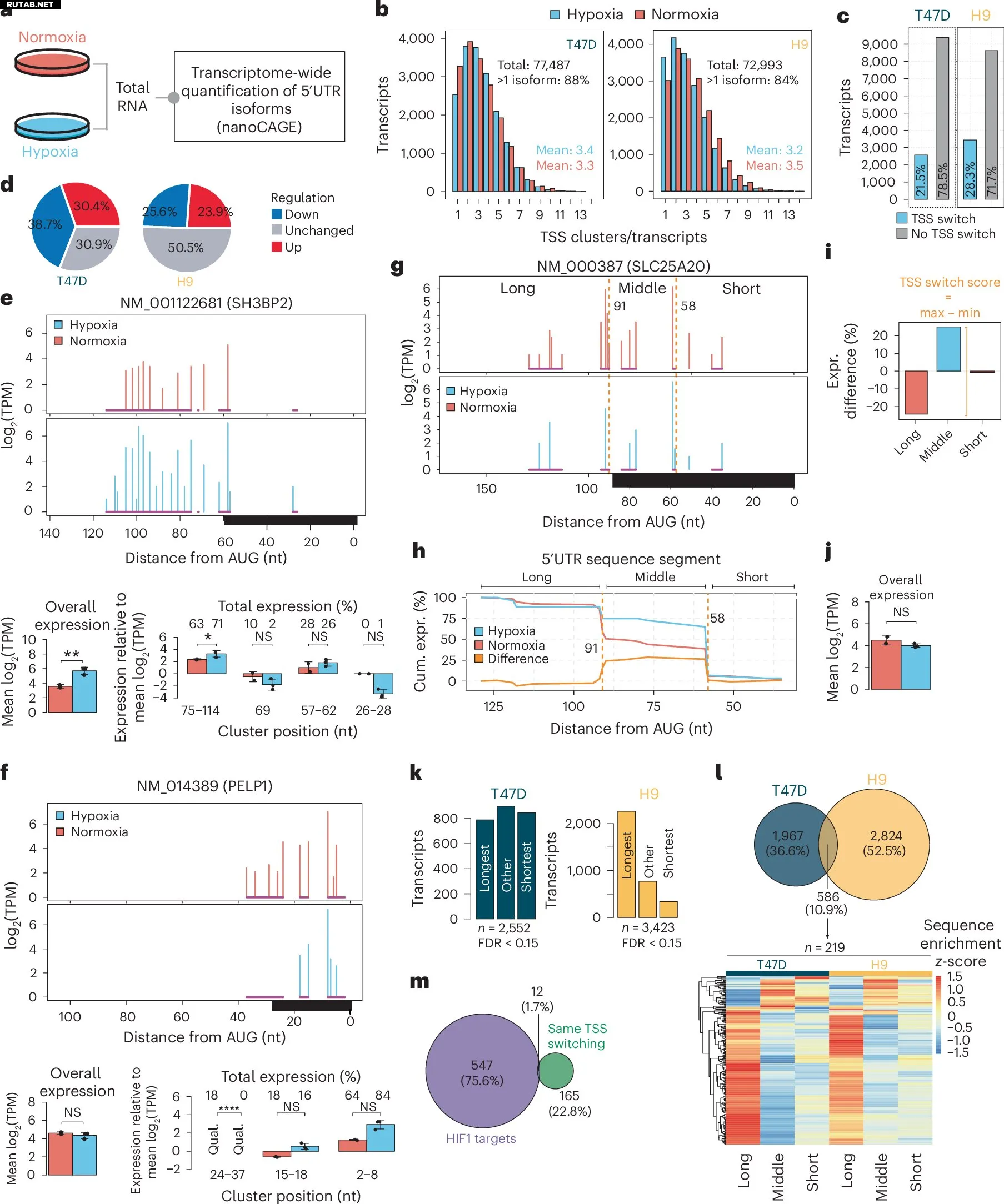
Гипоксия-индуцированное переключение TSS приводит к масштабной перестройке 5′UTR. Автор: Nature Cell Biology (2025). DOI: 10.1038/s41556-025-01786-8
Исследователи из Каролинского института обнаружили, как клетки могут регулировать активность своих генов, чтобы выжить при нехватке кислорода. Исследование, опубликованное в журнале Nature Cell Biology, раскрывает ранее неизвестный механизм, который клетки используют для контроля над тем, какие белки производятся и как быстро.
Когда клетки испытывают кислородное голодание, например, в опухоли или после травмы, они должны быстро адаптироваться, чтобы выжить. В новом исследовании учёные изучили, как эта адаптация работает на молекулярном уровне. Изучая клетки рака молочной железы и человеческие стволовые клетки, они обнаружили, что клетки переключают точку начала считывания генов — это влияет на эффективность производства белков.
«Мы увидели, что клетки в условиях гипоксии часто используют альтернативные стартовые сайты для регуляции генов, что меняет характеристики так называемой 5′UTR последовательности мРНК», — говорит Кэтлин Уотт, научный сотрудник отделения онкологии-патологии Каролинского института и первый автор исследования.
Эта последовательность действует как «разбег» перед началом формирования самого белка. Характеристики этих последовательностей контролируют, насколько эффективно клетка может производить белки. Исследователи обнаружили, что при низком уровне кислорода клетки часто выбирают другие версии 5′UTR, позволяя производить определённые важные белки более эффективно.
Одним из примеров является фермент PDK1, который помогает клетке переключить производство энергии с кислородозависимого процесса на процесс, работающий без кислорода — известный как гликолиз. Это ключевая стратегия выживания для клеток в стрессовых условиях.
Эпигенетика контролирует переключение
Исследователи также показали, что это переключение контролируется эпигенетическими изменениями — химическими модификациями в упаковке ДНК, которые влияют на активность генов. Было обнаружено, что специфическая модификация под названием H3K4me3 играет решающую роль. Воздействуя на эту модификацию с помощью лекарств, исследователи смогли заставить клетки изменить свои стартовые сайты генов — даже без изменения уровня кислорода.
«Это говорит о том, что эпигенетические изменения — не просто следствие гипоксии, а активная часть стратегии адаптации клетки», — говорит Кшиштоф Шкоп, научный сотрудник того же отделения и соавтор исследования.
Исследование даёт новое понимание того, как клетки регулируют производство белков в условиях стресса, и может быть важным для будущих исследований рака, поскольку опухолевые клетки часто живут в средах с низким содержанием кислорода.
«Это исследование — результат фантастического совместного усилия между нашей группой здесь, в Каролинском институте, и группой доктора Линн-Мари Постовит из Университета Куинс, вместе с нашими другими коллегами из Канады», — говорит Ола Ларссон, главный исследователь, также из отделения онкологии-патологии и соавтор исследования.
Больше информации: Кэтлин Уотт и др., Эпигенетические изменения способствуют транскрипционным и трансляционным программам при гипоксии, Nature Cell Biology (2025). DOI: 10.1038/s41556-025-01786-8
Источник: Karolinska Institutet









0 комментариев