Новый метод увеличивает производство белка в генетически модифицированных клетках
Исследователи из Уорикского университета разработали метод, позволяющий увеличить продолжительность работы и продуктивность «клеточных фабрик» — генетически модифицированных клеток, производящих химические вещества. Новый подход не требует применения антибиотиков или сложных методов инженерии.
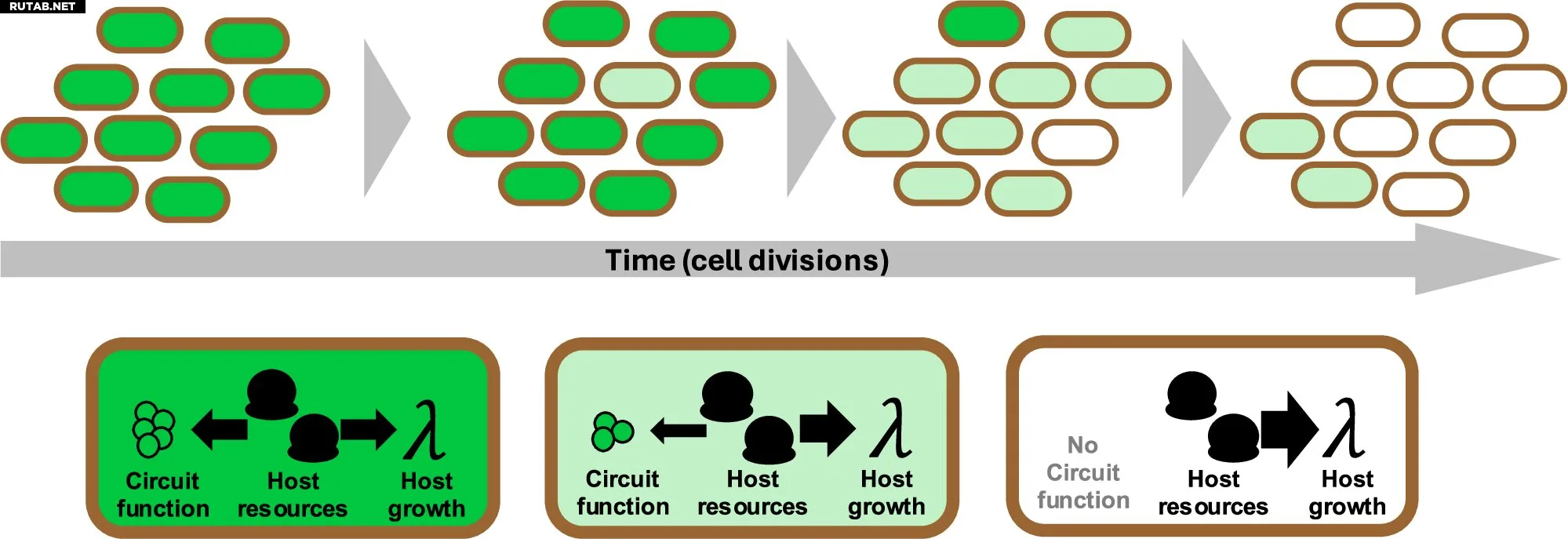
Схема, демонстрирующая потерю функции в генетически модифицированной популяции в процессе эволюции. Автор: Nature Communications (2025). DOI: 10.1038/s41467-025-63627-4
Синтетическая биология занимается созданием живых клеток, часто бактерий, которые функционируют как химические фабрики, производя вещества для здравоохранения, промышленности и экологии. Для этого в бактерии встраивают генетические схемы — синтетические ДНК-программы, которые заставляют клеточные механизмы производить нужные химикаты.
Однако существующие «живые фабрики» имеют ограниченный срок службы. Под нагрузкой производства клетки перестают функционировать, мутируют или проигрывают в конкуренции более быстрорастущим мутантным клеткам.
В статье, опубликованной в Nature Communications, учёные использовали компьютерное моделирование роста, мутации и конкуренции бактерий для поиска оптимального решения. Они оценили десятки стратегий генной инженерии, чтобы теоретически найти способ сохранить стабильность клеточных фабрик и обеспечить высокое производство на протяжении многих поколений.
Доктор Александр Дарлингтон, научный сотрудник Королевской инженерной академии и доцент Уорикского университета, объяснил: «Инженерные клетки имеют ограниченный срок жизни из-за стресса и генетических ошибок, приводящих к мутациям, которые разрушают функцию. Эти мутанты растут быстрее и быстро доминируют в клеточной фабрике».
«Мы применили идеи из технического регулирования, чтобы создать нечто вроде генетического термостата, который включает систему, когда она слишком холодная, и выключает, когда слишком горячая. Мы обнаружили, что лучшие результаты достигаются при комбинации двух саморегулирующихся систем обратной связи: одна чувствительна к производству, а другая — к скорости роста. Вместе эти системы с отрицательной обратной связью, согласно прогнозам, увеличивают функциональность наших инженерных клеток в три раза».
Оптимальная стратегия использует системы отрицательной обратной связи, вставляя гены, которые действуют как датчики, отслеживают скорость роста клеток и их продуктивность, а затем автоматически регулируют активность генов для поддержания стабильной работы. Небольшим недостатком является снижение скорости производства каждой клетки, но благодаря значительно более длительному сроку службы совокупное производство химических веществ со временем оказывается намного выше.
Предложенные подходы не требуют антибиотиков (что снижает риск развития устойчивости) или сложных инженерных усилий. Методы можно легко применять в различных системах без значительной переработки, что приближает к цели создания долговечных и надёжных приложений синтетической биологии.
Дополнительная информация: Daniel P. Byrom et al, Genetic controllers for enhancing the evolutionary longevity of synthetic gene circuits in bacteria, Nature Communications (2025). DOI: 10.1038/s41467-025-63627-4

0 комментариев