Ученые создали систему редактирования генома, способную переписывать целые главы ДНК
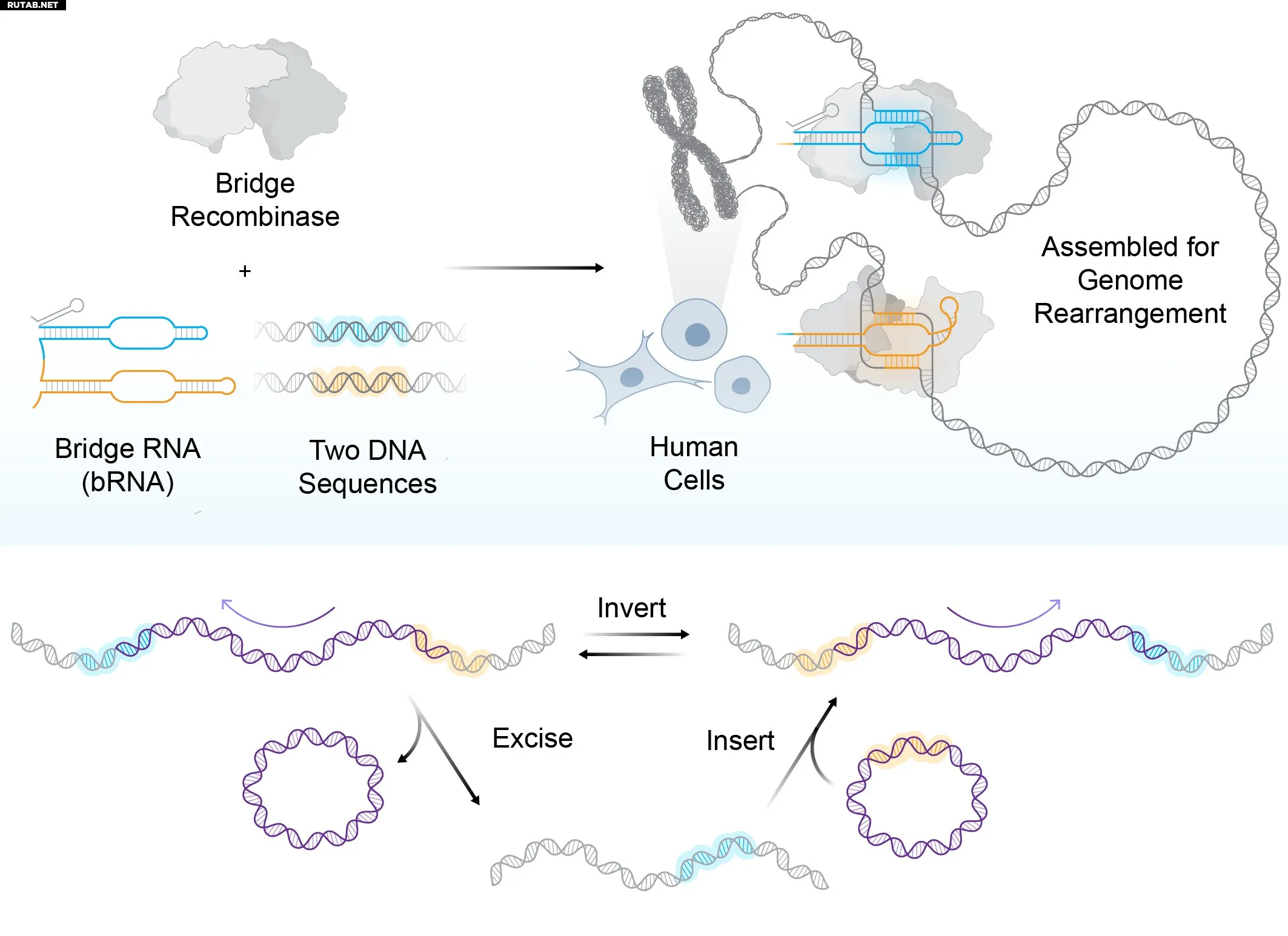
Схема, показывающая, как бридж-рекомбиназы с двойной системой наведения позволяют вставлять новый генетический материал, удалять нежелательные участки или переворачивать сегменты ДНК за один программируемый шаг. Автор: Кьяра Риччи-Там
Исследователи из Arc Institute представили универсальную систему редактирования генома, которая позволяет вырезать и вставлять целые «параграфы» ДНК, переставлять «главы» и даже перестраивать целые «пассажи» генетического кода. Работа опубликована в журнале Science.
Новая технология, названная бридж-рекомбиназами, позволяет манипулировать крупными участками генома длиной до миллиона пар оснований: вставлять новые гены, удалять целые кластеры генов или инвертировать регуляторные последовательности.
«Бридж-рекомбиназы могут трансформировать создание генетических терапий, предлагая одно универсальное лекарство для целой популяции пациентов вместо тысяч индивидуальных методов лечения», — заявил старший автор работы Патрик Сю, главный исследователь Arc Institute и профессор биоинженерии в Калифорнийском университете в Беркли.
«Способность перемещать и изменять целые генетические регионы позволяет нам конструировать биологию в том же масштабе, в котором работает эволюция, и применять эти возможности для решения сложных заболеваний».
В отличие от CRISPR, которая использует одну направляющую РНК для нацеливания на один участок ДНК, бридж-РНК уникальны тем, что могут одновременно распознавать две разные мишени в ДНК. Это позволяет системе выполнять скоординированные перестройки, например, сближать удаленные хромосомные регионы для удаления генетического материала или переворачивать последовательности.
В качестве доказательства концепции исследователи успешно удалили токсичные повторы ДНК, вызывающие атаксию Фридрейха — наследственное нейромышечное заболевание. В некоторых случаях система устранила более 80% патологических повторов.
«Поскольку тяжесть заболевания коррелирует с длиной повтора, любое удаление, даже если оно не приводит к полностью здоровому генотипу, имеет потенциал для улучшения симптомов у пациентов», — пояснил ведущий автор исследования Николас Перри.
Ученые также продемонстрировали, что технология может воспроизвести существующие терапевтические подходы, успешно удалив энхансер BCL11A — ту же мишень, что используется в одобренной FDA терапии серповидноклеточной анемии.
В настоящее время команда работает над расширением возможностей платформы, включая тестирование в клинически значимых иммунных клетках и стволовых клетках, а также разработку методов доставки терапии.
Больше информации: Nicholas T. Perry et al, Megabase-scale human genome rearrangement with programmable bridge recombinases, Science (2025). DOI: 10.1126/science.adz0276







0 комментариев