Ученые выяснили, как карбонаты влияют на превращение CO₂ в топливо
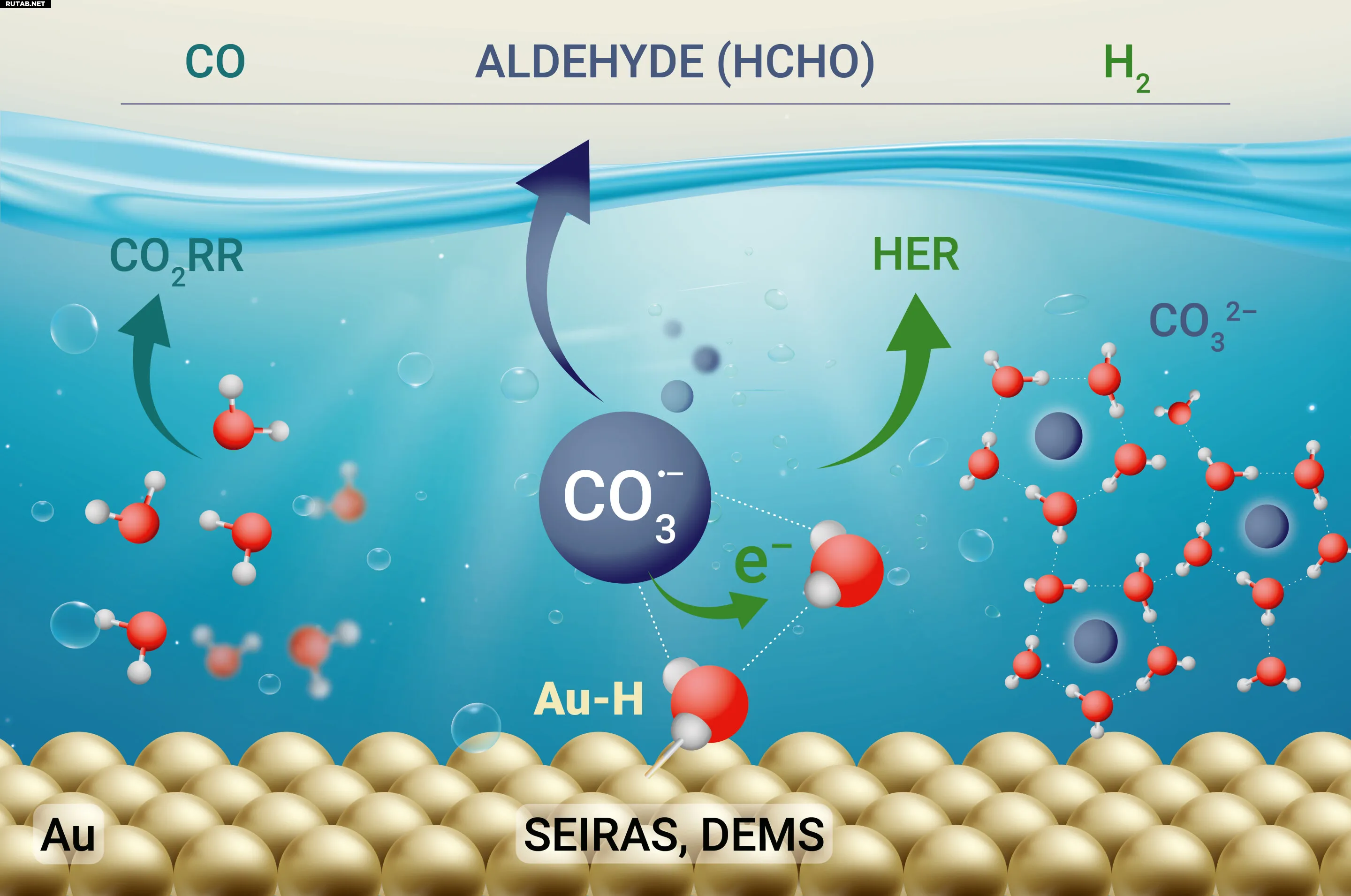
Роль карбонатов и их радикалов в электрохимическом восстановлении CO₂ и выделении водорода. Автор: Schleuse 01 / Maja Wypychowska
Исследователи из Центра Гельмгольца в Берлине (HZB) и Института Фрица Габера Общества Макса Планка (FHI) раскрыли, как молекулы карбоната влияют на преобразование CO₂ в ценные виды топлива с использованием золотых электрокатализаторов. Их открытия выявляют ключевые молекулярные механизмы в электрокатализе CO₂ и выделении водорода, указывая на новые стратегии повышения энергоэффективности и селективности реакции.
Работа опубликована в журнале Nature Chemistry.
Введение в электрохимическое восстановление CO₂
Превращение атмосферного CO₂ в топливо с помощью электрокатализа предлагает устойчивую альтернативу ископаемым ресурсам, но процесс остается неэффективным и дорогостоящим. Конкурирующие реакции, такие как выделение водорода, ограничивают производительность, а ключ к улучшению лежит на границе раздела фаз катализатора: гидратационные слои, формируемые водой и электролитами, регулируют эффективность этих химических превращений.
«Однако роль карбонат-анионов и природа гидратационных слоев на границе раздела во время электрохимического восстановления CO₂ до сих пор плохо изучены», — говорит доктор Кристофер Клей, руководитель Молодежной исследовательской группы Гельмгольца в HZB и отделе науки о границах раздела фаз в FHI.
Роль карбонатов и их радикалов
Чтобы ответить на эти вопросы, член команды Клея доктор Я-Вэй Чжоу разработала усовершенствованные спектроскопические методики, включая спектроскопию ИК-поглощения с ослабленным полным внутренним отражением и поверхностным усилением (ATR-SEIRAS).
«Это позволило нам обнаружить радикалы карбонат-анионов (CO₃•–), происходящие из гидратированного карбоната. Карбонаты способствуют молекулярному упорядочиванию в гидратационных слоях на границе раздела, а радикалы действуют как протонный реле и облегчают перенос заряда на золото, ускоряя выделение водорода», — объясняет доктор Чжоу, первый автор исследования.
Дальнейший анализ с использованием дифференциальной масс-спектрометрии (DEMS) показал, что карбонатные радикалы также являются источником углерода, производя формальдегид. Дополнительная спектроскопия с мечеными изотопами и моделирование методом функционала плотности (DFT), выполненные командой профессора Нурии Лопес в ICIQ в Таррагоне (Испания), подтвердили, что вода является основным донором протонов, а не бикарбонат, что проливает свет на давний спор в научной литературе.
Значение для будущих исследований
«Эти результаты дают новую перспективу на молекулярном уровне о конкуренции между электрохимическим восстановлением CO₂ и выделением водорода на золотых электродах, заставляя пересмотреть происхождение электрокаталитической селективности, которую необходимо изучить для таких материаловых систем, как медь, показавших более сложные тенденции селективности», — говорит профессор Беатрис Рольдан Куэнья из FHI.
Показав, как молекулы карбоната формируют локальную среду на поверхности катализатора, исследование подчеркивает стратегии повышения эффективности и селективности реакции, продвигая электрокаталитическое преобразование CO₂ и разработку более эффективных электрокаталитических систем для устойчивых энергетических применений.
Больше информации: Ya-Wei Zhou et al, Carbonate anions and radicals induce interfacial water ordering in CO₂ electroreduction on gold, Nature Chemistry (2025). DOI: 10.1038/s41557-025-01977-8
Источник: Max Planck Society
Электрокаталитическое восстановление CO₂ — одно из перспективных направлений в «зеленой» энергетике, позволяющее не только утилизировать парниковый газ, но и получать из него жидкое топливо. Золото, несмотря на свою высокую стоимость, часто используется в фундаментальных исследованиях в качестве модельного катализатора благодаря своей химической стабильности и предсказуемому поведению в реакциях.




0 комментариев