Новый наноматериал на основе графена улучшает точность доставки лекарств от рака
Исследователи разработали pH-чувствительный наноматериал на основе оксида графена, полиглицерина и DMMA, который меняет заряд в кислой среде, что позволяет ему прикрепляться к опухолевым клеткам. Автор: Профессор Юта Нишина из Университета Окаямы
Рак остается одной из основных причин смерти во всем мире, и, несмотря на достижения в диагностике и лечении, он продолжает оказывать значительное влияние на глобальное здоровье. Ученые начали исследовать инновационные методы, такие как инженерные наноматериалы (ENMs), способные обеспечить целенаправленную доставку лекарств к раковым клеткам. Однако поведение pH-чувствительных наноматериалов в организме, где они постоянно взаимодействуют с биологическими жидкостями, до сих пор изучено недостаточно.
Чтобы восполнить этот пробел, команда исследователей под руководством профессора Юты Нишины из Исследовательского института междисциплинарных наук Университета Окаямы (Япония) совместно с доцентом Яцзюань Цзоу и профессором Альберто Бьянко из CNRS Университета Страсбурга (Франция) изучила, как pH-чувствительные наноматериалы меняют свои свойства и взаимодействуют с белками и клетками in vivo. Результаты исследования были опубликованы 1 июня 2025 года в журнале Small.
Оксид графена — углеродный наноматериал, получаемый из графита, — в последнее время стал популярен в нанотехнологиях благодаря своей структуре и способности накапливаться в опухолях за счет эффекта повышенной проницаемости и удержания. Однако его применение ограничено тем, что иммунная система быстро удаляет его из кровотока, что снижает эффективность поглощения раковыми клетками.
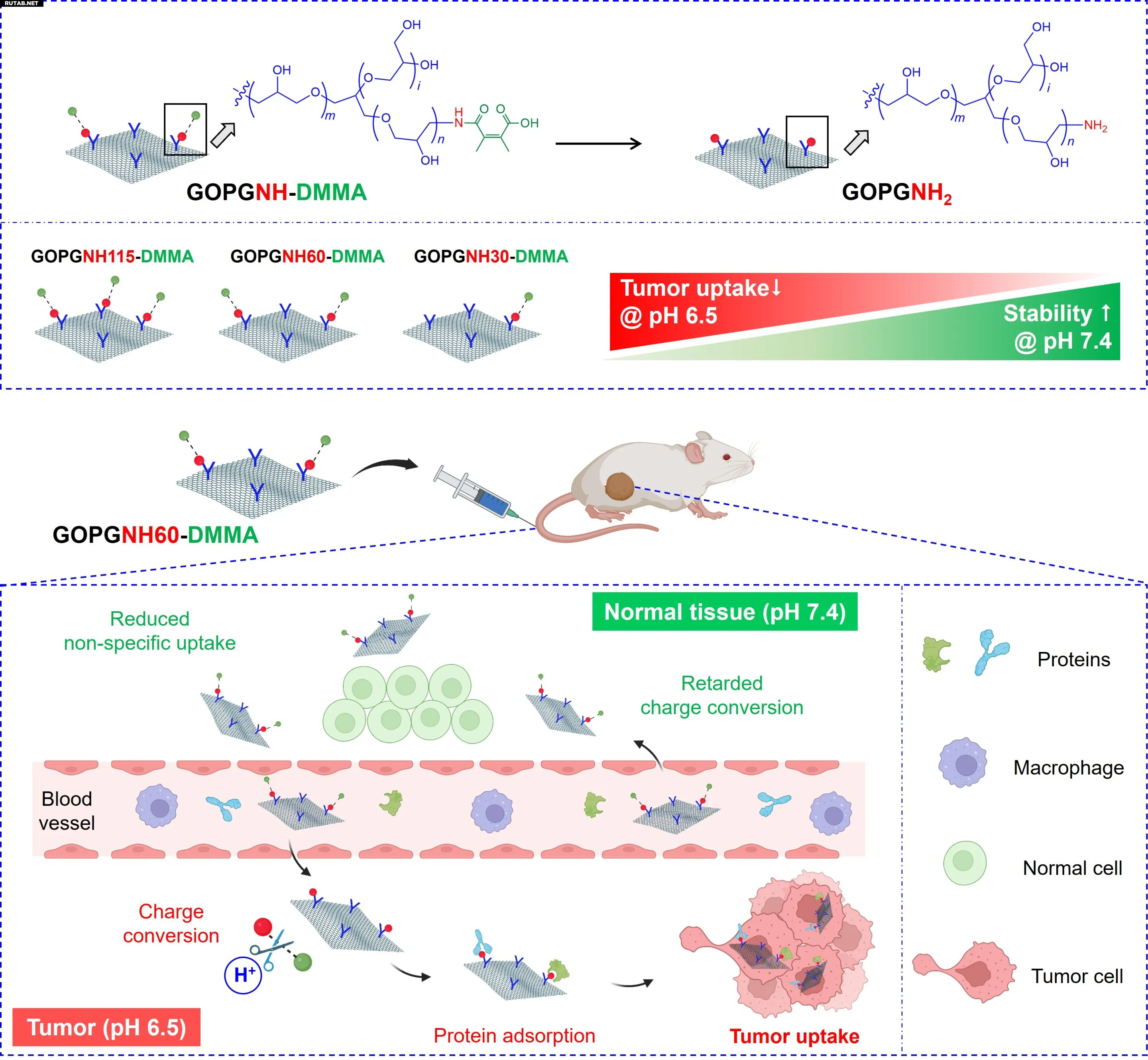
Чтобы решить эту проблему, ученые разработали «переключаемый» графеновый материал, присоединив к листам оксида графена гиперразветвленный полимер — амино-богатый полиглицерин (hPGNH2), а затем добавив группу диметилмалеинового ангидрида (DMMA), чтобы сделать поверхность pH-чувствительной.
«Когда материал находится в нейтральной среде кровотока, его поверхность остается отрицательно заряженной, избегая обнаружения иммунной системой, — объясняет профессор Нишина. — Но при попадании в слабокислую среду опухоли его заряд становится положительным, что помогает ему связываться с раковыми клетками и проникать в них».
Команда проанализировала три версии этого материала (GOPG-DMMA), варьируя плотность аминогрупп в hPGNH2: GOPGNH115, GOPGNH60 и GOPGNH30. Разница в количестве аминогрупп влияла на итоговый положительный заряд и, следовательно, на способность материала прикрепляться к клеткам.
Результаты показали, что вариант GOPGNH60-DMMA оказался наиболее эффективным, обеспечивая баланс между безопасностью в кровотоке и оптимальным положительным зарядом в кислой среде опухоли. Это позволило материалу эффективнее достигать раковых клеток, избегая при этом связывания со здоровыми клетками и белками крови. Кроме того, он демонстрировал более высокое накопление в опухолях с меньшими побочными эффектами, что подтвердилось в экспериментах на мышах.
«Мы обнаружили, что, регулируя поверхностную химию, можно контролировать поведение наноматериалов в организме, — говорит доктор Цзоу. — Успех этого точного контроля может открыть новые возможности для "тераностики", объединяющей диагностику и лечение рака».
Исследование стало важным шагом в развитии целевой доставки лекарств и может помочь оптимизировать pH-чувствительные наноматериалы для большей точности. Полученные данные также могут улучшить доставку препаратов внутрь клеток, особенно в кислых компартментах, таких как лизосомы и эндосомы, что сделает лечение более точным и снизит вред для здоровых тканей.
Работа является частью международного сотрудничества: в 2025 году Университет Окаямы и CNRS запустили программу IRP C3M, направленную на создание "умных" наноматериалов для здравоохранения. В будущем исследователи продолжат расширять границы применения наноматериалов для улучшения терапии.
«Теперь у нас есть четкие рекомендации по улучшению эффективности pH-чувствительных нанопрепаратов, — говорит профессор Нишина. — С этим открытием мы на шаг ближе к будущему персонализированной медицины».
Дополнительная информация: Yajuan Zou et al, Polyglycerol‐Grafted Graphene Oxide with pH‐Responsive Charge‐Convertible Surface to Dynamically Control the Nanobiointeractions for Enhanced in Vivo Tumor Internalization, Small (2025). DOI: 10.1002/smll.202503029
Источник: Okayama University



0 комментариев