Ученые нашли общую уязвимость у вирусов полиомиелита и простуды
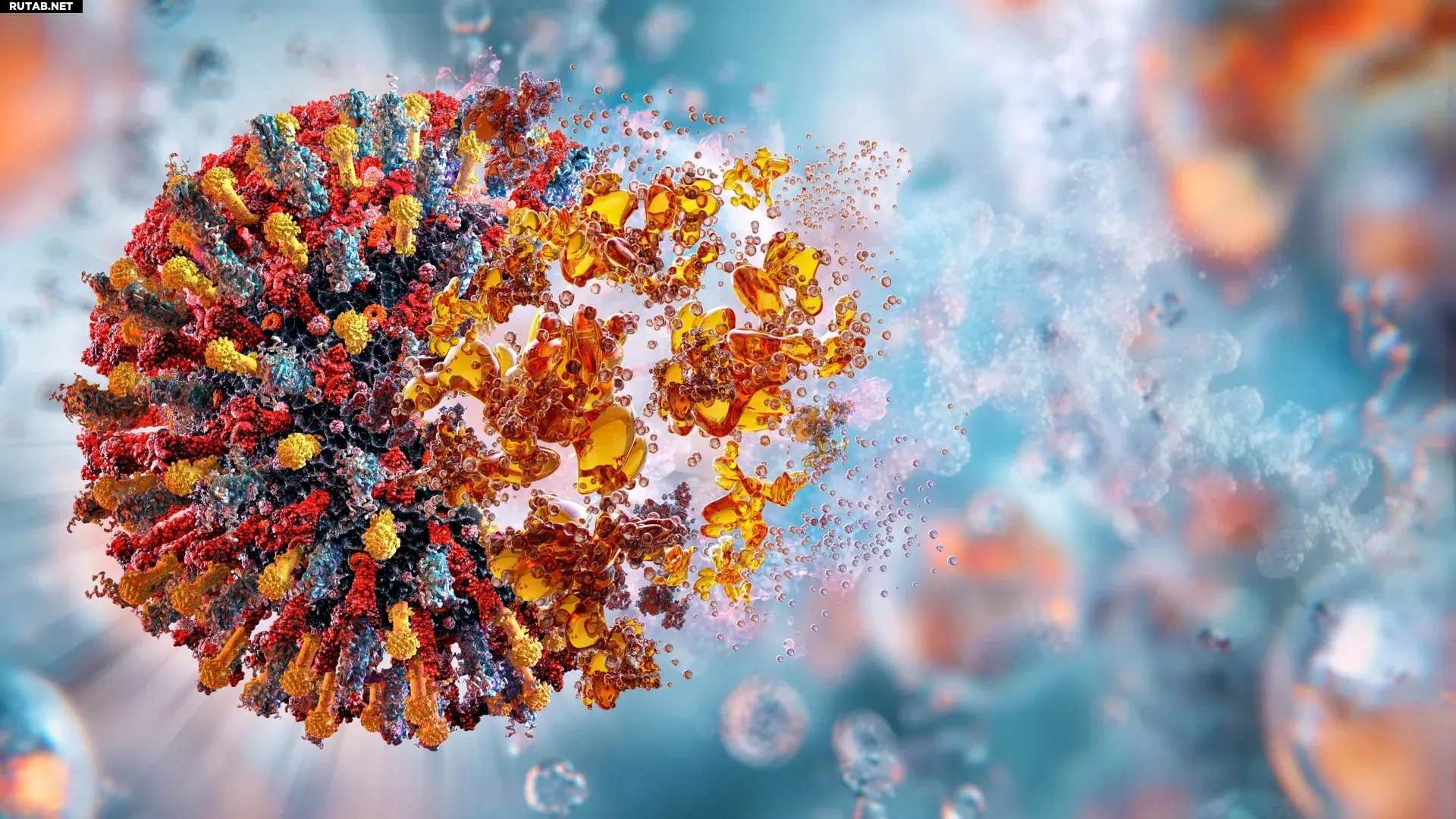
Новое исследование раскрывает молекулярный механизм, который энтеровирусы используют для захвата клеток человека и размножения, выявляя критическую уязвимость вирусов, связанных с полиомиелитом, миокардитом и простудой. Credit: Shutterstock
Исследователи из Университета Мэриленда в Балтиморе (UMBC) обнаружили ключевой этап, который энтеровирусы используют для размножения внутри клеток человека. Результаты, опубликованные в журнале Nature Communications, объясняют, как вирусы, вызывающие такие заболевания, как полиомиелит, энцефалит, миокардит и даже обычная простуда, берут под контроль клеточные механизмы для своего копирования. Ученые полагают, что это открытие может помочь в создании нового поколения противовирусных препаратов, способных одновременно воздействовать на множество энтеровирусов.
Исследование провели Дипак Койрала, доцент кафедры химии и биохимии UMBC, и недавний выпускник докторантуры Наба Кришна Дас. Их работа помогает ответить на давние вопросы о том, как эти вирусы запускают репликацию после проникновения в клетку.
«Моя лаборатория была очень мотивирована понять, как РНК-вирусы производят свои белки внутри клетки и размножают свой геном, чтобы создавать больше вирусных частиц», — говорит Койрала. Более ранняя работа команды выявила важную структуру в форме клеверного листа внутри вирусной РНК. Новое исследование показывает, как эта структура привлекает белки, необходимые для построения вирусного репликационного механизма.
Как энтеровирусы размножаются внутри клеток
Энтеровирусы имеют очень маленькие РНК-геномы, которые должны выполнять две задачи одновременно. Вирусная РНК должна направлять производство вирусных белков, а также служить шаблоном для создания новых копий вируса.
Большая часть вирусного генома содержит инструкции для структурных белков, но также кодирует несколько специализированных белков, необходимых для репликации. Одним из наиболее важных является гибридный белок 3CD.
Часть 3C разрезает длинные цепочки аминокислот на отдельные белки, необходимые вирусу. Часть 3D действует как РНК-полимераза — фермент, копирующий вирусную РНК, чтобы вирус мог размножаться. Клетки человека естественным образом не содержат такой полимеразы, поэтому вирус должен поставлять свою собственную версию.
«Ранее мы определили структуру только РНК, а другие группы определили структуру 3C и 3D, но теперь мы зафиксировали структуру РНК и белков вместе, поэтому мы знаем, как они взаимодействуют», — объясняет Койрала. «Мы обнаружили, что именно домен 3C белка 3CD связывается с РНК в вирусном геноме, а затем привлекает другие компоненты, такие как клеточный белок PCBP2, для сборки репликационного комплекса».
Исследователи также обнаружили, что этот молекулярный комплекс работает как переключатель. Когда 3CD присоединен, вирус копирует свой РНК-геном. Когда белок отсоединяется, РНК становится доступной для производства вирусных белков.
Ученые разрешили давнюю вирусную загадку
Чтобы детально изучить эти взаимодействия, команда использовала рентгеновскую кристаллографию для визуализации РНК-клеверного листа и белка 3CD вместе. Они также использовали изотермическую титрационную калориметрию (ITC), которая измеряет тепло, выделяемое при связывании молекул, и биослойную интерферометрию (BLI), которая использует изменения интерференции света для отслеживания того, как долго молекулы остаются связанными.
Эксперименты помогли разрешить продолжающийся научный спор. Исследователи показали, что две полные молекулы 3CD, каждая со своей собственной РНК-полимеразой, связываются бок о бок на вирусной РНК. Более ранние исследования предполагали, что белки вместо этого образуют единую слитую пару.
Ученые до сих пор не до конца понимают, почему требуются две копии, но новое исследование дает гораздо более четкую картину того, как начинается процесс репликации.
Потенциал для широкоспектрых противовирусных препаратов
Одним из самых многообещающих результатов стало то, насколько похожим оказался механизм у всех семи энтеровирусов, изученных в исследовании. Вирусы имели почти идентичные структуры РНК-клеверного листа и поведение при связывании.
Такой уровень сходства предполагает, что структура РНК чрезвычайно важна для выживания вируса. Значительные мутации, вероятно, нарушили бы репликацию, что делает эту структуру потенциально стабильной мишенью для лекарств против многих энтеровирусов.
Исследователи говорят, что это открывает возможность разработки противовирусных препаратов широкого спектра действия, которые могли бы работать против целого семейства вирусов, а не против одного патогена.
Ученые уже разрабатывают лекарства, которые мешают работе белков 3C и 3D, но новые результаты открывают еще одну возможную стратегию.
«Лекарства, нарушающие активность 3C и 3D, уже разрабатываются, но теперь у нас есть еще один уровень для тестирования», — говорит Койрала. «Что, если мы нацелимся на РНК или на интерфейс РНК-белок, чтобы разорвать взаимодействие? Это еще одна возможность. Теперь, когда у нас есть структуры высокого разрешения, мы можем точно разрабатывать молекулы лекарств для воздействия на них».
Койрала отмечает, что исследование подчеркивает, насколько удивительно сложными могут быть вирусы, несмотря на их крошечные геномы.
«Вирусы очень, очень умны. Их полный геном эквивалентен примерно одной последовательности мРНК у человека, но они настолько эффективны», — говорит Койрала. Его последняя работа демонстрирует, «почему нам нужно изучать эту фундаментальную науку — чтобы ее можно было применить для разработки лекарств, нацеленных на патогены, вызывающие так много вредных заболеваний».
Источники:
sciencedaily.com
Материалы предоставлены Университетом Мэриленда в Балтиморе.
Naba Krishna Das, Alisha Patel, Reem Abdelghani, Deepak Koirala. Structural basis for 3C and 3CD recruitment by enteroviral genomes during negative-strand RNA synthesis. Nature Communications, 2025; 16 (1) DOI: 10.1038/s41467-025-64376-0





0 комментариев