Ученые раскрыли новые механизмы движения бактерий и обмена ДНК
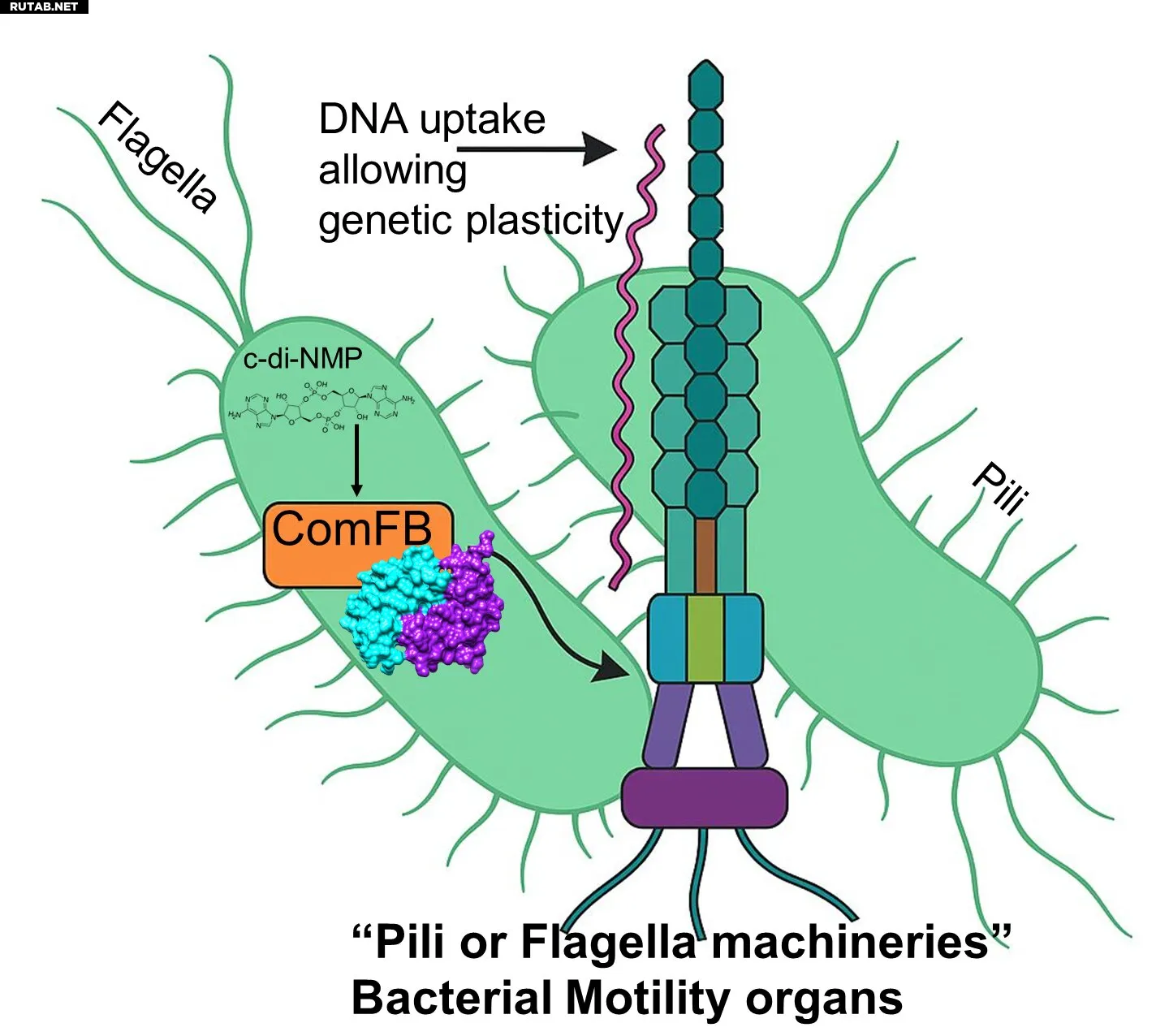
Механизм сократительного пилуса, который позволяет бактериям двигаться, регулируется сигналами c-di-AMP через рецепторный белок ComFB. Этот механизм позволяет передавать ДНК от одной бактерии к другой. Автор: HHU / Халед Селим—изображение, созданное ИИ
Бактерии постоянно перемещаются с помощью органов движения, называемых жгутиками или пилусами, чтобы колонизировать новые ниши. Кроме того, бактерии могут обмениваться информацией, как бы «разговаривая друг с другом», и таким образом приобретать новые способности посредством обмена материалами ДНК.
Эти органы движения играют важную роль в поглощении ДНК для обмена генетической информацией между разными бактериями, обеспечивая так называемую геномную пластичность. Следовательно, органы движения бактерий вносят вклад в патогенность бактерий, колонизацию хозяев, формирование биопленок и распространение устойчивости к антибиотикам.
В совместных исследованиях ученые из Университета Генриха Гейне в Дюссельдорфе (HHU), Тюбингенского университета, а также университетов Гиссена, Фрайбурга, Института биологии Макса Планка в Тюбингене, Национальных институтов здоровья США и Медицинской школы Нью-Джерси обнаружили новое семейство сигнальных белков, широко распространенное в бактериальном царстве и способствующее регуляции механизмов движения бактерий и поглощения ДНК.
Исследователи сообщили о своем открытии в двух публикациях в журналах Cell Discovery и Proceedings of the National Academy of Sciences.
В этих двух исследованиях команда под руководством профессора доктора Халеда Селима (Институт фототрофной микробиологии при HHU и кластер передового опыта CMFI в Тюбингене) выявила, что молекулы вторичных мессенджеров (c-di-GMP и c-di-AMP) вместе с недавно обнаруженным рецепторным белком ComFB регулируют как движение бактерий, так и поглощение ДНК, следовательно, возможно, способствуя патогенности бактерий.
Аспирант Шерихан Самир, первый автор обеих публикаций, заявила: «Способность различных белков ComFB из различных бактерий связывать и точно интегрировать сигнал(ы) движения/поглощения ДНК регулируется вторичными мессенджерами динуклеотидами (c-di-GMP и c-di-AMP)».
Эти характеристики были обнаружены у цианобактерий, Bacillus subtilis и Vibrio cholerae, возбудителя вспышек холеры.
Профессор Селим сказал: «c-di-AMP принадлежит к одному из относительно недавно открытых классов циклических динуклеотидных вторичных мессенджеров, чьи клеточные функции еще не до конца поняты. В этих исследованиях мы показываем, что белки ComFB чувствуют c-di-AMP, а также c-di-GMP и необходимы для регуляции естественной компетентности и движения бактерий».
Термин «естественная компетентность» описывает способность бактериальных клеток поглощать молекулы ДНК и интегрировать их в свой собственный геном для обмена генетической информацией между собой. Этот процесс, например, в основном способствует распространению устойчивости к антибиотикам от изначально лишь нескольких бактерий на целые популяции, а также через границы разных видов.
До сих пор неясно, какие другие группы бактерий — помимо изученных — также используют этот механизм. «Если патогенные бактерии, имеющие клиническое значение, также используют его, это может проложить путь к новым стратегиям борьбы с мультирезистентными бактериями», — сказал Селим.
ИИ: Открытие нового семейства сигнальных белков ComFB, регулирующих ключевые процессы у бактерий, — это значительный шаг в фундаментальной микробиологии. Понимание того, как именно бактерии обмениваются генами устойчивости к антибиотикам, может в перспективе помочь в разработке принципиально новых подходов к борьбе с супербактериями, что крайне актуально в 2025 году.
Больше информации: Sherihan Samir et al, ComFB, a widespread family of c-di-NMP receptor proteins, Proceedings of the National Academy of Sciences (2025). DOI: 10.1073/pnas.2513041122
Sherihan Samir et al, The second messenger c-di-AMP controls natural competence via ComFB signaling protein, Cell Discovery (2025). DOI: 10.1038/s41421-025-00816-x
Источник: Heinrich-Heine University Duesseldorf







0 комментариев