Учёные разработали метод прогнозирования заражения C. difficile до появления симптомов
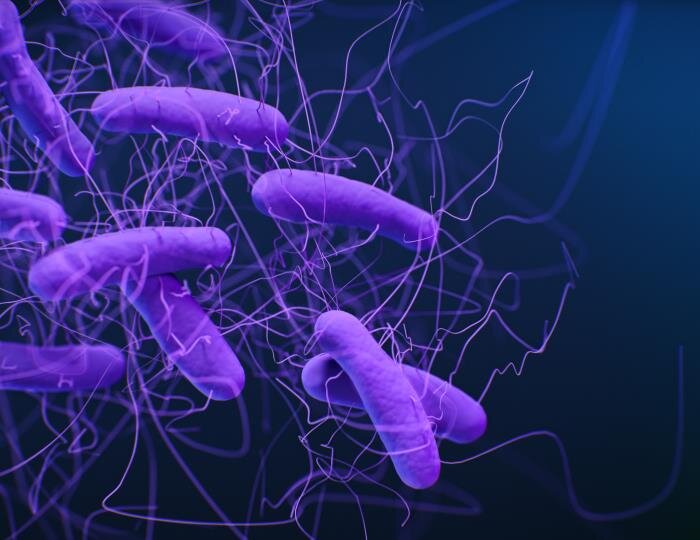
Медицинская иллюстрация бактерий Clostridioides difficile (ранее известных как Clostridium difficile) из публикации Центров по контролю и профилактике заболеваний США (CDC) «Угрозы устойчивости к антибиотикам в США, 2019». Автор: CDC
Clostridioides difficile (C. difficile) — коварная угроза. Эта бактерия ежегодно заражает более 500 000 человек в США и убивает до 30 000. Она является одной из основных причин внутрибольничных инфекций, особенно в стационарах и учреждениях длительного ухода. Однако не все носители C. difficile заболевают — до 30–40% населения имеют эту бактерию в кишечнике, не испытывая симптомов.
C. difficile — это так называемый оппортунистический патоген: он может вызывать опасные для жизни заболевания, но также способен мирно существовать в кишечнике, ожидая подходящего момента (например, после курса антибиотиков), чтобы начать разрушительную деятельность.
А что, если бы мы могли выявлять риск до начала заражения?
В новом исследовании, опубликованном в журнале Cell Systems, учёные из Института системной биологии (ISB) разработали персонализированную модель, позволяющую прогнозировать вероятность колонизации кишечника C. difficile и тестировать эффективность пробиотиков для предотвращения или устранения этой колонизации.
«C. difficile — оппортунист. Он может скрываться в кишечнике, живя безвредно, готовый вызвать болезнь при подходящих условиях. Если мы устраним возможность, мы нейтрализуем угрозу», — говорит доктор Шон Гиббонс, старший автор исследования и доцент ISB.
Команда использовала метаболические модели микробных сообществ, разработанные соавтором исследования доктором Кристианом Динером, чтобы смоделировать поведение C. difficile в более чем 15 000 образцах микробиоты кишечника человека. Модели выявили три состояния колонизации: высокий рост, умеренный рост и отсутствие роста — в зависимости от уникального состава микробиоты каждого человека.
Эксперименты с искусственными сообществами кишечных бактерий показали, что модель точно предсказывает, какие сообщества уязвимы для C. difficile, а какие устойчивы. Кроме того, исследователи успешно предсказали колонизацию у пациентов с рецидивирующей инфекцией до и после трансплантации фекальной микробиоты.
Учёные также обнаружили, что определённый коктейль пробиотиков подавляет рост C. difficile, конкурируя за ключевые метаболиты, такие как сукцинат, трегалоза и орнитин. Однако эффективность пробиотиков зависела от состава микробиоты, что указывает на необходимость персонализированного подхода.
«Эта работа приближает нас к созданию точных пробиотиков — индивидуальных вмешательств, учитывающих экосистему кишечника каждого человека», — говорит доктор Алекс Карр, ведущий автор исследования.
Результаты открывают путь к снижению числа инфекций C. difficile и потенциально могут быть применены для управления другими оппортунистическими патогенами. Однако предложенные методы ещё предстоит проверить в клинических испытаниях.
Дополнительная информация: Personalized Clostridioides difficile colonization risk prediction and probiotic therapy assessment in the human gut, Cell Systems (2025). DOI: 10.1016/j.cels.2025.101367






0 комментариев