Фрагмент дифтерийного токсина сливает липидные везикулы при нейтральном pH
Исследователи из Швейцарского нанонаучного института (SNI) обнаружили новый способ слияния липидных везикул при нейтральном pH. Используя фрагмент дифтерийного токсина, команда добилась слияния мембран везикул без предварительной обработки или жестких условий. Их работа, опубликованная в журнале Communications Chemistry, открывает путь к новым применениям в технологиях «лаборатория-на-чипе», биосенсорах и искусственных клеточных прототипах.
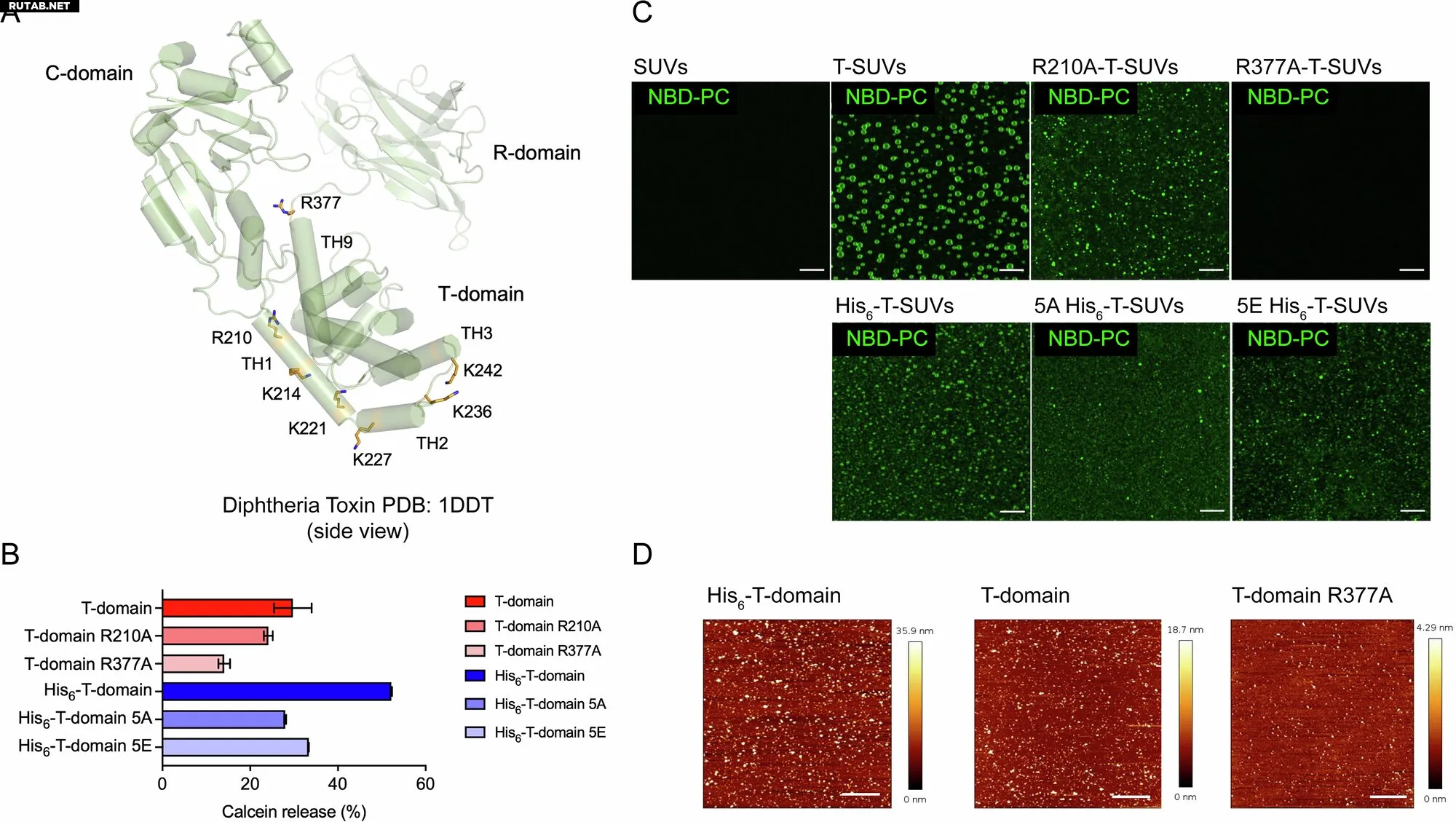
Роль основных аминокислотных остатков в слиянии везикул, опосредованном T-доменом. Автор: Communications Chemistry (2025). DOI: 10.1038/s42004-025-01738-1
Липидные везикулы — крошечные сферы, окруженные мембранами, — являются важными инструментами в медицине и нанотехнологиях. Они могут транспортировать фармацевтические агенты к специфическим клеткам и тканям или содержать контрастные вещества для диагностических исследований. Контролируемое слияние позволяет создавать более крупные отсеки, имитирующие сложность живых клеток.
Дифтерийный токсин обеспечивает слияние мембран
Исследовательская группа под руководством профессора Корнелии Паливан из Университета Базеля и доктора Ричарда А. Каммерера из Института Пауля Шеррера достигла прорыва в белковом слиянии мембран в лаборатории с использованием дифтерийного токсина.
«Конкретная часть дифтерийного токсина, известная как T-домен, может индуцировать слияние мембран даже при нейтральном pH — без необходимости функционализации мембран везикул во время производства. Это уникально, поскольку обычно этот токсин работает в кислых условиях внутри клеток», — поясняет Пётр Ясько, первый автор исследования и докторант Швейцарского нанонаучного института.
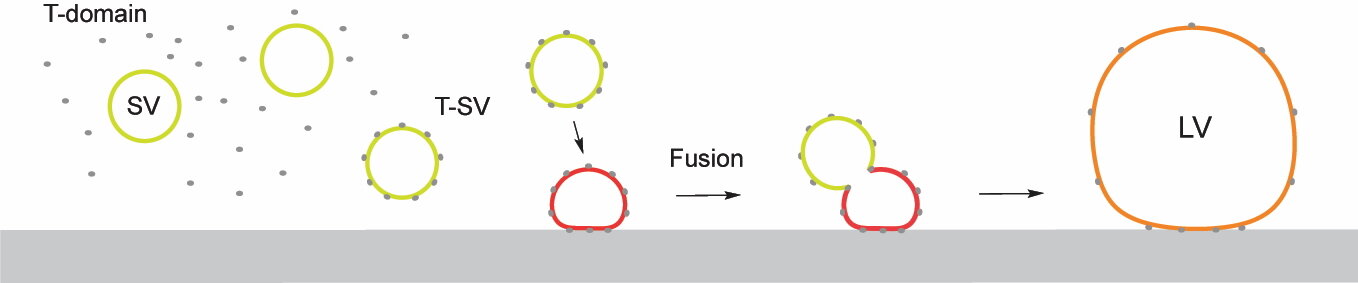
Специфические положительно заряженные аминокислоты домена дифтерийного токсина (серые точки) связываются с отрицательно заряженными мембранами везикул. Это приводит к асимметричному натяжению мембраны (красный цвет). Когда другие свободно плавающие везикулы в растворе сливаются с присоединенной везикулой, натяжение мембраны снижается и образуются более крупные везикулы. Автор: P. Jasko, University of Basel and PSI
Положительно заряженные аминокислоты критичны
Определенные положительно заряженные аминокислоты в дифтерийном белке играют роль в слиянии при нейтральном pH. Аминокислоты связываются с отрицательно заряженной мембраной везикулы, что позволяет везикулам адсорбироваться на стеклянной поверхности.
Возникающее асимметричное натяжение мембраны является триггером, который затем приводит к слиянию присоединенных и свободно плавающих частиц, что сопровождается снижением мембранного натяжения.
«В зависимости от силы положительного заряда на T-домене или количества отрицательно заряженных липидов, слияние производит множество мелких или меньше крупных везикул, которые во всех случаях сохраняют свою сферическую форму», — объясняет Каммерер.
«Целевое слияние мембран при нейтральном pH представляет для нас большой интерес, поскольку может использоваться для многочисленных приложений. Это обеспечивает основу для различных технологий «лаборатория-на-чипе», биосенсоров и возможного использования с синтетическими аналогами липосом», — комментирует Паливан.






0 комментариев