Учёные разработали быстрый метод поиска генетических «переключателей»
Автор: Cell Genomics (2025). DOI: 10.1016/j.xgen.2025.100984
Исследователи из Центра молекулярной медицины имени Макса Дельбрюка разработали новый метод для изучения того, как ДНК управляет генами. Их методика, опубликованная в журнале Cell Genomics, позволяет быстрее, чем существующие методы, выявлять генетические «переключатели», регулирующие важные гены.
Большая часть человеческого генома не кодирует белки. Вместо этого она состоит из регуляторных областей. Подобно выключателям, которые включают и выключают свет, эти области нуклеотидов — называемые транскрипционными энхансерами — определяют, где и когда ген активен, и в значительной степени контролируют, сколько соответствующего белка производит клетка.
Дефекты в генетическом коде таких регуляторных элементов могут вызывать нарушения развития и заболевания. Но по сравнению с кодирующими белки областями их трудно идентифицировать, поскольку они часто расположены далеко от регулируемых генов и не имеют четко определенного генетического кода.
Учёные под руководством доктора Дубравки Вучичевич из лаборатории вычислительной и регуляторной геномики профессора Уве Олера создали мощный новый инструмент для обнаружения этих областей, контролирующих наши гены.
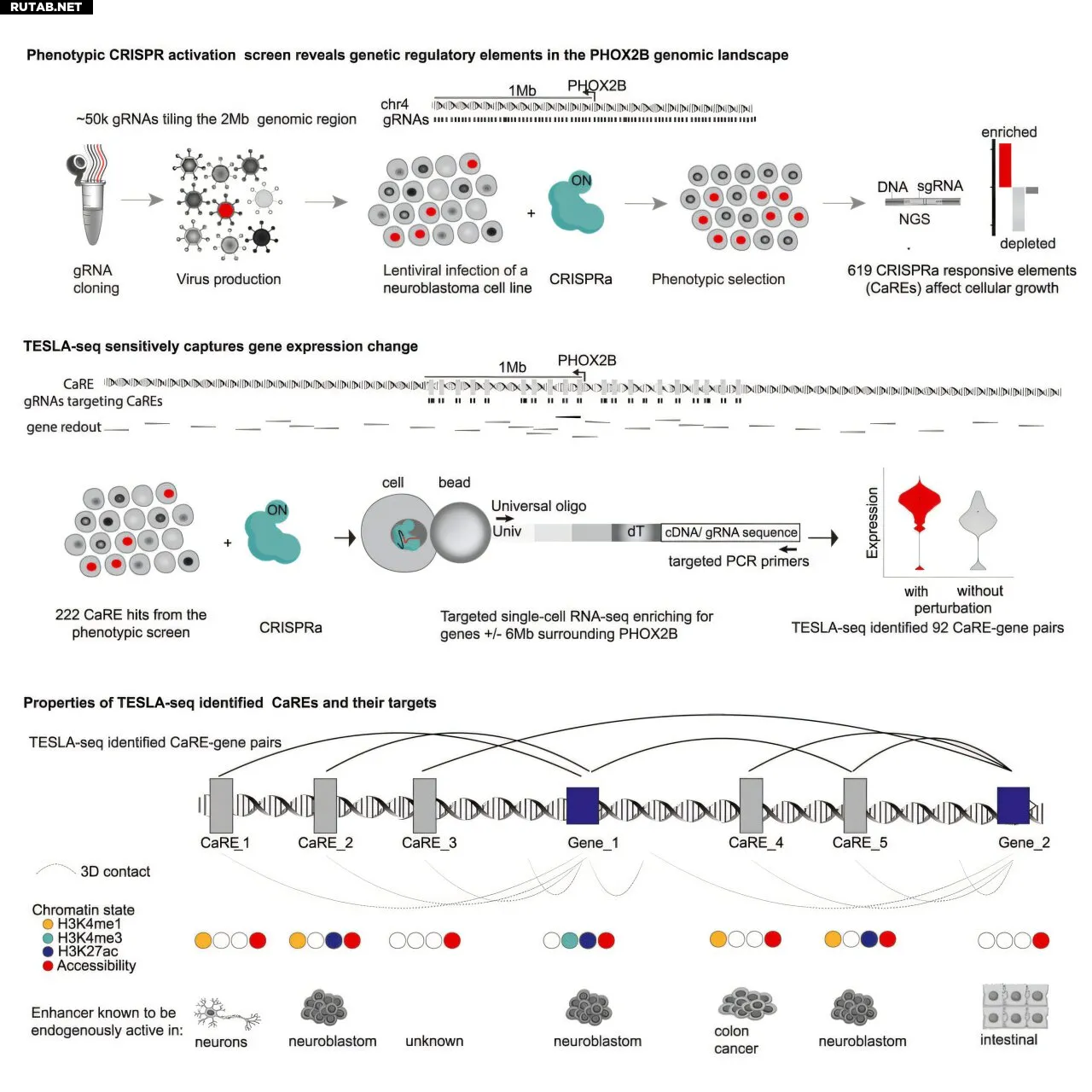
Метод под названием TESLA-seq (таргетированный скрининг активации на уровне одной клетки) сочетает активацию генов на основе CRISPR (CRISPRa) — технику регуляции генов, использующую модифицированную систему CRISPR-Cas9 для усиления экспрессии конкретных генов — и таргетированное секвенирование РНК единичных клеток для более быстрого и точного выявления регуляторных областей по сравнению с другими методами.
«С помощью этого метода мы можем фактически проверить, как тысячи кандидатных регуляторных элементов в геноме способны включать гены — и выяснить, на какие именно гены они влияют», — говорит Вучичевич, ведущий автор исследования.
Картирование регуляторных элементов
Чтобы продемонстрировать технику, исследование сосредоточилось на гене PHOX2B, который необходим для развития нервной системы. Мутации в этом гене связывают с нейробластомой — раком ткани нервной системы, который в основном поражает детей.
Учёные сконцентрировались на большой области вокруг PHOX2B, разработав по 2–3 направляющих РНК (gRNA) для каждого 100-парного сегмента ДНК, всего 46 722 gRNA. Этот набор исследовал весь геномный ландшафт гена PHOX2B, а также других соседних генов, на предмет потенциальной роли в качестве регуляторных переключателей.
Затем каждую gRNA перенесли в отдельную клетку человеческой нейробластомы. gRNA указывала системе CRISPRa, куда направляться, и активировала любые регуляторные области, которые могли присутствовать в «сегменте». Было идентифицировано более 600 областей — называемых CaREs (элементы, реагирующие на CRISPRa) — которые при активации изменяли рост клеток.
Затем команда подробнее изучила около 200 CaREs и использовала таргетированное секвенирование РНК единичных клеток, чтобы считать как gRNA внутри каждой клетки, так и РНК, экспрессируемую из близлежащих генов. Это позволило связать каждый CaRE с любым из более чем 70 генов в области PHOX2B, экспрессия которых изменялась в этой клетке. Также были обнаружены прямые связи между CaREs и важными регуляторами SHISA3 и APBB2, которые участвуют в развитии рака и болезни Альцгеймера.
Неожиданно оказалось, что многие CaREs контролируют удалённые гены, полностью пропуская близлежащие — это то, что другие методы часто упускают.
«TESLA-seq не просто фиксирует то, что происходит в одном типе клеток, он может выявлять потенциальные связи между генами и регуляторными областями в различных биологических системах», — говорит Олер.
Это важно, поскольку многие заболевания затрагивают более чем один тип ткани, добавляет Вучичевич.
«Метод можно использовать для изучения обширных, неисследованных частей нашей ДНК, которые влияют на здоровье и болезни в нескольких системах органов, и он может помочь нам разрабатывать более точные и эффективные методы лечения».
Больше информации: Sensitive dissection of a genomic regulatory landscape using bulk and targeted single-cell activation, Cell Genomics (2025). DOI: 10.1016/j.xgen.2025.100984



0 комментариев