Новый вычислительный фреймворк от Harvard SEAS раскрывает генетические правила самоорганизации клеток
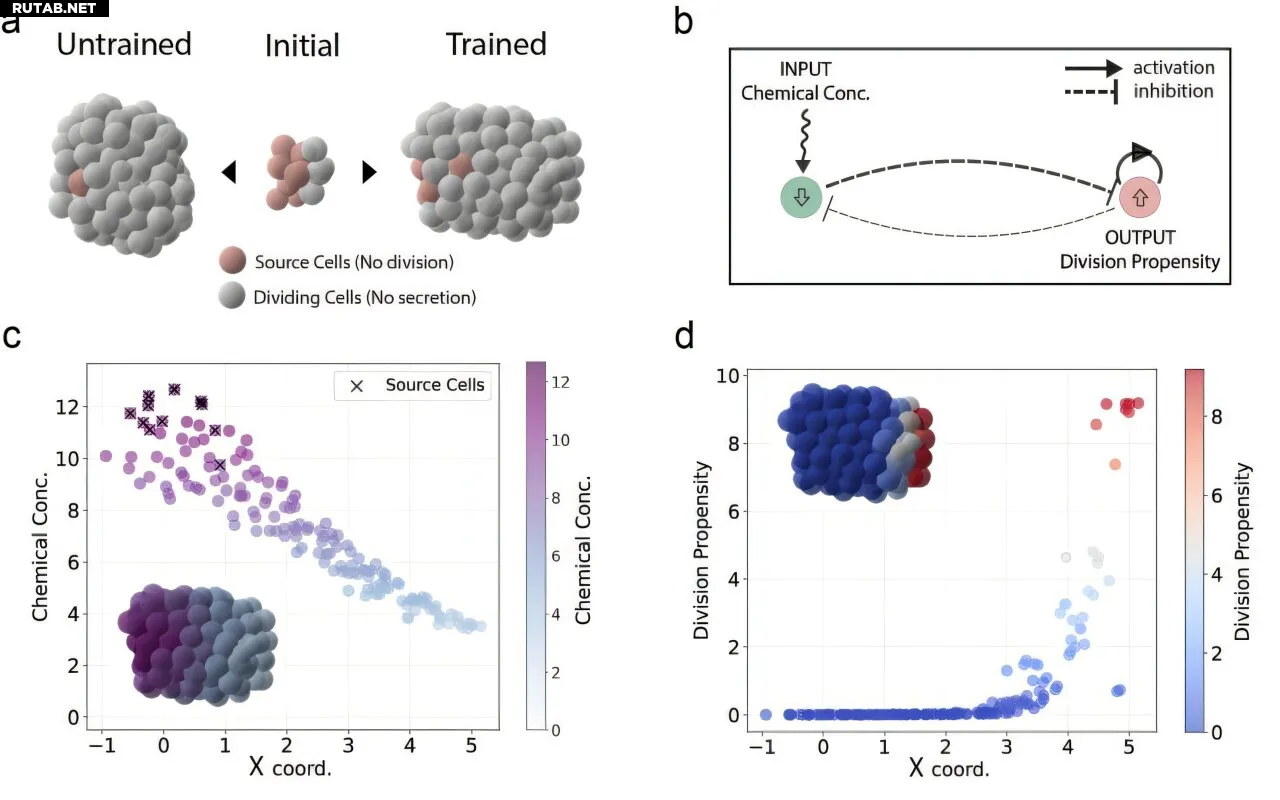
Схема горизонтального удлинения в оптимизированном клеточном кластере. (а) Слева: конечная конфигурация симуляции со случайно инициализированными параметрами; справа: конечное состояние симуляции после обучения. Клетки-источники, выделенные красным, секретируют фактор роста и не могут делиться. Пролиферирующие клетки, серые, чувствуют фактор роста и делятся в ответ на него. (b) Изученная генная сеть. Ген рецептора активируется только присутствием внешнего химического фактора, что приводит к подавлению склонности к делению. (c) Химический градиент, создаваемый клетками-источниками вдоль x-координаты кластера. (d) Распределение склонности к делению в конце симуляции вдоль оси x, показывающее концентрацию делящихся клеток на кончике. Автор: Nature Computational Science (2025). DOI: 10.1038/s43588-025-00851-4
Одним из самых фундаментальных процессов во всей биологии является спонтанная организация клеток в кластеры, которые делятся и в конечном итоге превращаются в формы — будь то органы, крылья или конечности.
Ученые давно исследуют этот невероятно сложный процесс для создания искусственных органов или понимания роста раковых опухолей, но точное проектирование отдельных клеток для достижения желаемого коллективного результата часто является процессом проб и ошибок.
Прикладные физики из Гарварда рассматривают контроль клеточной организации и морфогенеза как проблему оптимизации, которую можно решить с помощью мощных новых инструментов машинного обучения. В новом исследовании, опубликованном в Nature Computational Science, исследователи из Школы инженерии и прикладных наук имени Джона А. Полсона (SEAS) создали вычислительный фреймворк, который может извлекать правила, которым клетки должны следовать по мере роста, чтобы из целого возникала коллективная функция.
Компьютер изучает эти «правила» в форме генетических сетей, которые направляют поведение клетки, влияя на множество способов химической сигнализации между клетками или физические силы, которые заставляют их слипаться или отталкиваться.
В настоящее время являясь доказательством концепции, новые методы могут быть объединены с экспериментами, чтобы позволить ученым понимать и контролировать, как организмы развиваются на клеточном уровне.
Исследование было совместно проведено аспиранткой Рамьей Дешпанде и постдокторантом Франческо Моттесом. Старшим автором выступил Майкл Бреннер, профессор прикладной математики и прикладной физики в SEAS.
Автоматическое дифференцирование
Поиск правил, которым должны следовать клетки, стал возможен благодаря вычислительной технике, называемой автоматическим дифференцированием. Этот метод, который составляет основу обучения моделей глубокого обучения в искусственном интеллекте, состоит из алгоритмов, предназначенных для эффективного вычисления высокосложные функции. Автоматическое дифференцирование позволяет компьютеру обнаружить точный эффект, который небольшое изменение в любой части генной сети окажет на поведение всего клеточного коллектива.
В течение последних нескольких лет команда Бреннера применяет такие алгоритмы к задачам, выходящим за рамки нейронных сетей, включая проектирование самосборных коллоидных материалов, улучшение гидродинамического моделирования и конструирование определённых типов белков.
Дешпанде заявила, что принципы из статьи могут помочь направить последующие эксперименты на физических системах клеток.
«Как только у вас есть модель, которая может предсказать, что произойдет, когда у вас будет определенная комбинация клеток, генов или молекул, которые взаимодействуют, можем ли мы затем инвертировать эту модель и сказать: "Мы хотим, чтобы эти клетки собрались вместе и сделали эту конкретную вещь. Как нам запрограммировать их на это?"
Моттес сказал, что, обеспечивая масштабирование физически обоснованных моделей системной биологии, автоматическое дифференцирование предлагает многообещающий путь к достижению прогнозирующего контроля, необходимого для того, чтобы в отдаленном будущем инженеры могли управлять ростом органов — святой Грааль вычислительной биоинженерии.
«Если у вас есть модель, которая достаточно предсказуема и достаточно откалибрована на экспериментальных данных, надежда заключается в том, что вы можете просто сказать, например: "Я хочу сфероид с такими характеристиками. Как мне следует сконструировать свои клетки, чтобы достичь этого?"— сказал Моттес.
Больше информации: Ramya Deshpande et al, Engineering morphogenesis of cell clusters with differentiable programming, Nature Computational Science (2025). DOI: 10.1038/s43588-025-00851-4
Источник: Harvard University




0 комментариев