ИИ и CRISPR объединились для точного редактирования генов
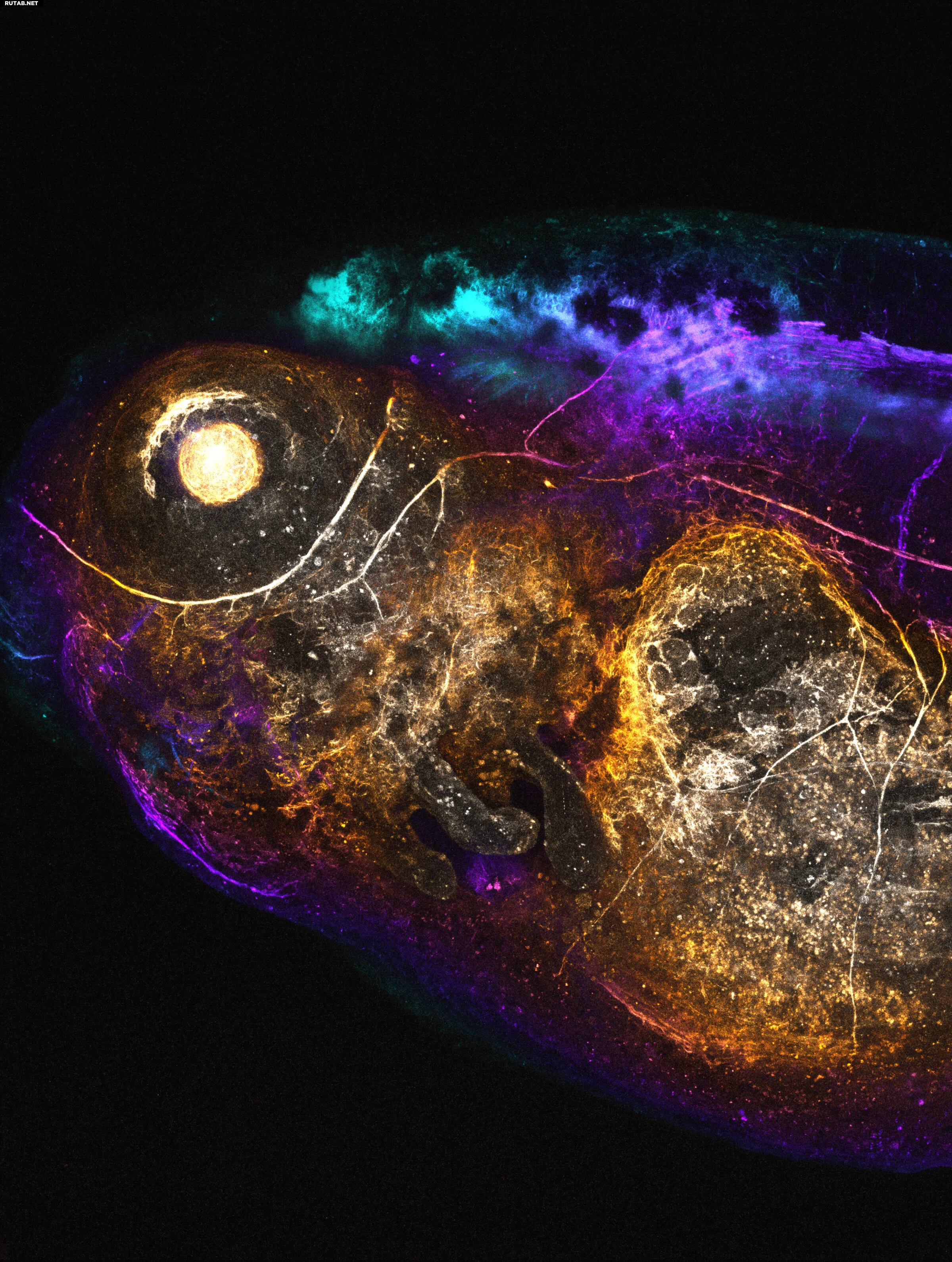
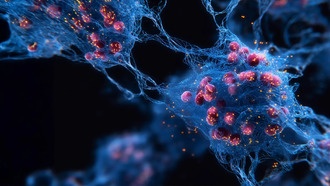
Флуоресцентно меченная нейромолекула в живом головастике, где цвета обозначают глубину визуализации. Мозг и спинномозговые нервы видны в верхней части (бирюзовый и фиолетовый), а путь периферических нервов прослеживается по всему телу головастика. Автор: Тайо Ямамото, Университет Цюриха
Исследовательская группа под руководством Университета Цюриха разработала новый мощный метод точного редактирования ДНК, объединив передовые технологии генной инженерии с искусственным интеллектом. Работа была опубликована в журнале Nature Biotechnology.
Эта технология открывает путь к более точному моделированию человеческих заболеваний и закладывает основу для генной терапии следующего поколения.
Точное и направленное редактирование ДНК с помощью точечных мутаций, а также интеграция целых генов с использованием технологии CRISPR/Cas, имеет огромный потенциал для применения в биотехнологии и генной терапии. Однако критически важно, чтобы «генетические ножницы» не вызывали нежелательных изменений в геноме, сохраняя его целостность и избегая побочных эффектов.
Генное редактирование с повышенной точностью
Ученые из Университета Цюриха (UZH), Гентского университета (Бельгия) и ETH Zurich разработали новый метод, значительно повышающий точность редактирования генома. Инструмент под названием «Пифия» (Pythia) с помощью искусственного интеллекта (ИИ) предсказывает, как клетки будут восстанавливать свою ДНК после разрезания CRISPR/Cas9.
«Наша команда создала крошечные шаблоны для репарации ДНК, которые действуют как молекулярный клей и направляют клетку для внесения точных генетических изменений», — говорит ведущий автор Томас Нарт, разработавший технологию в UZH и сейчас работающий в Гентском университете.
Эти шаблоны, спроектированные ИИ, сначала протестировали на культурах человеческих клеток, где они обеспечили высокоточное редактирование и интеграцию генов. Метод также подтвердил свою эффективность на других организмах, включая лягушку Xenopus (используемую в биомедицинских исследованиях) и живых мышах, где ученые успешно отредактировали ДНК в клетках мозга.
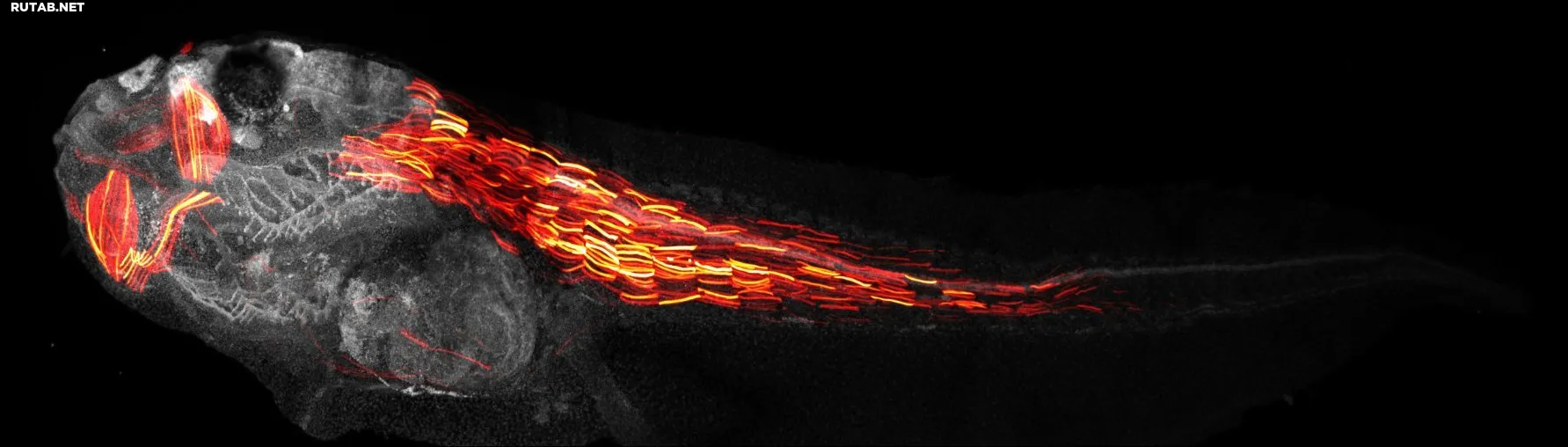
3D-визуализация производства красного флуоресцентного белка в головастике. Ген, ответственный за его синтез, активируется только в мышечных клетках. Автор: Тайо Ямамото, Университет Цюриха
ИИ учится предсказывать механизмы репарации ДНК
«Репарация ДНК следует определенным закономерностям, а не происходит случайно. И Пифия использует эти закономерности в наших интересах», — объясняет Нарт.
Традиционно после разрезания ДНК CRISPR ученые полагаются на естественные механизмы восстановления клетки. Хотя эти процессы предсказуемы, они могут приводить к нежелательным последствиям, например, повреждению соседних генов.
«Мы смоделировали в огромном масштабе, что процесс репарации ДНК подчиняется четким правилам, которые ИИ может изучить и предсказать», — говорит Нарт.
На основе этих данных исследователи с помощью машинного обучения смоделировали миллионы возможных исходов редактирования, задав простой, но мощный вопрос: как наиболее эффективно внести конкретное изменение в геном, учитывая вероятный механизм восстановления клетки?
Метод позволяет не только изменять отдельные «буквы» генетического кода или встраивать внешние гены, но и маркировать определенные белки флуоресцентными метками.
«Это невероятно мощный инструмент, потому что он позволяет напрямую наблюдать, что делают отдельные белки в здоровых и больных тканях», — отмечает Нарт.
Еще одно преимущество метода — его эффективность во всех типах клеток, включая неделящиеся, например, в нейронах мозга.
Основа для безопасной генной терапии
Название «Пифия» отсылает к жрице Дельфийского оракула, предсказывавшей будущее. Аналогичным образом новый инструмент позволяет ученым с высокой точностью прогнозировать результаты генного редактирования.
«Как метеорологи используют ИИ для прогнозирования погоды, мы применяем его для предсказания реакции клеток на генетические вмешательства. Такая предсказательная сила необходима, чтобы сделать редактирование генов безопасным, надежным и клинически полезным», — говорит профессор Университета Цюриха и ETH Zurich Зёрен Линкамп, старший автор исследования.
Работа открывает новые возможности для изучения генетических заболеваний и разработки более безопасных и эффективных методов генной терапии, в том числе для неврологических болезней.
Дополнительная информация: Precise, predictable genome integrations by deep learning–assisted design of microhomology-based templates, Nature Biotechnology (2025). DOI: 10.1038/s41587-025-02771-0. www.nature.com/articles/s41587-025-02771-0
Источник: University of Zurich




0 комментариев